Mit Freie-Elektronen-Lasern wie der LCLS könnten sich die Strukturinformationen auch aus Partikeln kitzeln lassen, die sich herkömmlichen Strukturmethoden einschließlich der Röntgenstruktur-Analyse verweigern. Ein Großteil aller Biomoleküle – darunter viele, die als Zielmoleküle medizinischer Therapien in Frage kommen – lassen sich nämlich nicht als Kristalle züchten. Ein einzelnes Protein-Molekül aber liefert in der konventionellen Röntgenstrukturanalyse kein erkennbares Signal.
Streuprozess muss Strahlenschaden zuvorkommen
Um auch von Einzelmolekülen messbare Signale zu erhalten, muss also die die Intensität der Röntgenstrahlung drastisch erhöht werden, wobei allerdings die Belichtungsdauer so kurz sein muss, dass der Röntgenpuls die Probe passiert, bevor es zu Strahlenschäden kommt. „Der Streuprozess muss also dem Strahlenschaden zuvorkommen, ihm sozusagen vorweg laufen“, sagt Schlichting, die Max-Planck-Institut für medizinische Forschung tätig ist.
Ob sich die Hoffnung der Forscher erfüllen wird, ist noch nicht ausgemacht. Denn die große Stärke des Röntgenlasers ist auch seine Schwäche: Mit seiner extrem hohen Intensität bildet der Strahl nicht nur den Aufbau der Moleküle ab, sondern zerstört sie auch, und zwar innerhalb von zehn Femtosekunden, also im Hunderttausendsten Bruchteil einer Milliardstel Sekunde. Fragt sich nur, ob die Teilchen vorher noch die Signale aussenden können, die etwas über ihre Struktur verraten.
„Theoretische Studien deuten darauf hin, dass das funktioniert, wenn die Pulse des Lasers noch kürzer sind als der Zerfallsprozess“, sagt Daniel Rolles von der ASG, der dieser Frage unter anderem nachgeht. Tatsächlich haben die Partner am LCLS die Dauer der Pulse inzwischen unter sieben Femtosekunden gedrückt. „Ob die theoretischen Voraussagen zutreffen, werden uns aber erst die Experimente verraten.“
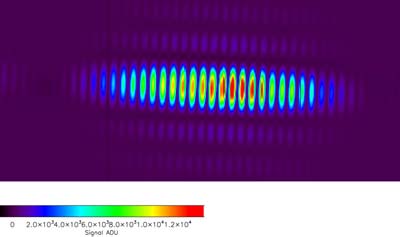
Interferenzmuster auf dem CCD Detektor von einem Doppelspalt, der mit FLASH Licht bestrahlt wurde. © MPI Halbleiterlabor / Strüder
Xenon-Cluster mit Röntgenlaser untersucht
Das zu klären, ist ein Zweck der ersten Experimente mit dem CAMP-Instrument an der LCLS, die im September 2009 den Betrieb aufgenommen hat. So haben Wissenschaftler der ASG gemeinsam mit Forschern um Thomas Möller von der Technischen Universität (TU) Berlin und um Christoph Bostedt von SLAC Xenon-Cluster mit dem Röntgenlaser untersucht. Dabei haben sie auch grundlegende Erkenntnisse darüber gewonnen, wie sich die Teilchen mit den Röntgenblitzen treffen lassen und welche Informationen die Teilchen dabei über ihre Struktur preisgeben.
„Die Experimente an Clustern liefern einen Einblick in die Wechselwirkung der extrem intensiven Lichtpulse mit den Nanoteilchen, die praktisch sofort nach der Abbildung zerfallen“, erläutert Möller. „Mit unseren Experimenten schaffen wir Grundlagenwissen, das helfen wird, auch andere Nanoteilchen mit einem Röntgenlaser zu untersuchen.“ In einem nächsten Schritt, im Juni 2010, wird ein internationales Team um Schlichting biologische Proben in der CAMP Apparatur untersuchen.
Wie Moleküle zerplatzen
Um die Moleküle möglichst vor der zerstörerischen Kraft des Röntgen-Lasers zu schützen, wollen die Forscher zudem herausfinden, wie sie zerplatzen. Genau dabei hilft ihnen das CAMP-Instrument, das mit zahlreichen ausgeklügelten Spektrometern ausgestattet ist. Das vier Millionen Euro teure Gerät enthält die weltweit größten und schnellsten Röntgen-CCD-Chips, die Energie und Intensität des gestreuten Lichts messen. Die Chips haben Wissenschaftler um Strüder im MPI Halbleiterlabor gebaut.
„Die Chips lassen sich 200 Mal in der Sekunde auslesen, schneller als der Röntgenlaser überhaupt feuert, können wir also das Signal jedes einzelnen Pulses detektieren“, erklärt Robert Hartmann, einer der Forscher, die die Chips konstruiert haben.
Mechanismus der Zerstörung im Visier
„Neben dem Röntgenlicht das durch die Moleküle gebeugt wird und ein aufschlussreiches Muster erzeugt, fangen die CCDs Detektoren auch das Licht ein, das die Moleküle abgeben, nachdem sie das Röntgen-Licht absorbiert haben“, erklärt Sascha Epp von der ASG, der die Detektoren in CAMP eingebaut hat. Diese Signale geben den Forschern Hinweise, wie die Teilchen zertrümmert werden. Auf den Mechanismus der Zerstörung lassen zudem die Bruchstücke schließen, in die das untersuchte Molekül zerfällt und die CAMP ebenfalls einsammelt.
„Mit einem sehr genauen Flugzeit-Massenspektrometer messen wir sowohl die Massen der Fragmente als auch ihre Impulse“, sagt Artem Rudenko, einer der ASG Wissenschaftler der dieses Reaktionsmikroskop maßgeblich mitentwickelt hat, und Ullrich ergänzt: „Wir können die Bruchstücke also identifizieren und erfahren gleichzeitig, wie schnell sie in welche Richtung aus dem Molekül geschleudert wurden.“ Genau diese Erkenntnisse könnten helfen, die Teilchen, die der Laser ins Visier nimmt, so in eine Matrix einzubetten, dass der Laser möglichst wenig Schaden anrichtet.
Teile des Instruments haben die Forscher schon mit FLASH getestet, einem Freie-Elektronen-Laser am Deutschen Elektronen-Synchrotron (DESY), der hochenergetisches UV-Licht abstrahlt. Dort haben sie unter anderem die Abbildungstechniken, den CCD Detektor sowie das Reaktions-Mikroskop entwickelt und untersucht, wie die Detektoren auf intensive Lichtblitze reagieren.
Pulse wirbeln Elektronen durcheinander
„CAMP ist so erfolgreich, dass fast ein Drittel der bisher am LCLS genehmigten Experimente damit gemacht werden“, so Ullrich. Denn mit den vielen unterschiedlichen Informationen, die CAMP über die Streuexperimente liefert, lassen sich nicht nur die Strukturuntersuchungen optimieren. „Wir lernen daraus auch etwas über die grundlegenden Prozesse, die extrem intensive Röntgen-Pulse in den Molekülen anstoßen.“
Fest steht, dass diese Pulse die Elektronen in den Molekülen völlig durcheinander wirbeln. Nur wie, das wissen die Physiker noch nicht. Diese Prozesse zu verstehen, trägt letztlich dazu bei, mehr über die Funktionen der Moleküle zu lernen und sie medizinisch oder technisch auszunutzen.
(Max-Planck-Gesellschaft, 23.02.2010 – DLO)
23. Februar 2010