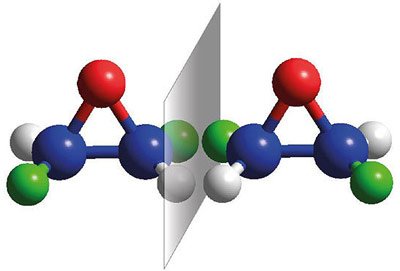
Kleiner Unterschied, große Wirkung: Die meisten biologischen Moleküle kommen in zwei Varianten vor, die sich gegenseitig Original und Spiegelbild sind. Sie verhalten sich also wie die rechte und die linke Hand zueinander. Nun haben Heidelberger Wissenschaftler eine Methode entwickelt, die gewissermaßen Schnappschüsse von chiralen Molekülen macht und somit deren räumlichen atomaren Aufbau direkt sichtbar macht.
Links riecht anders als Rechts
Forscher sprechen bei Molekülen, die in zwei zueinander spiegelbildlichen Formen vorkommen, von „chiralen“ Molekülen. Viele biologische Prozesse hängen entscheidend davon ab, ob die beteiligten organischen Moleküle links- oder rechtshändig sind. Zum Beispiel lassen die links- und rechtshändigen Varianten des gleichen Moleküls Zitronen und Orangen unterschiedlich riechen. Auch in der Pharmazie kann die Händigkeit eines Stoffes für seine Wirkung eine wichtige Rolle spielen. Wissenschaftler wollen deshalb wissen, wie die Atome in den beteiligten Molekülen relativ zueinander angeordnet sind. In der Fachsprache nennt sich das absolute Konfiguration. Aus dieser lässt sich die Händigkeit des Moleküls ablesen.
Zwar gibt es durchaus Methoden, um die Händigkeit chiraler Moleküle zu bestimmen. Doch diese liefern nicht die absolute Konfiguration ohne Verwendung theoretischer Modelle. Außerdem gab es bislang kein Messverfahren, das einzelne chirale Moleküle im gasförmigen Zustand auf ihre Händigkeit untersuchen konnte. Chemiker und Physiker aus Heidelberg haben nun erstmals den Chiralitätssinn einer gasförmigen Probe, eines chiralen Epoxides, durch direkte Abbildung seiner Molekülstruktur bestimmt.
Dazu haben zunächst die Chemiker um Oliver Trapp von der Ruprecht-Karls-Universität eine Verbindung mit definierter Händigkeit hergestellt, ein chirales Molekül namens Dideuterooxiran. Kleinste Mengen davon verwendeten anschließend Kreckel und seine Kollegen in stark verdünnten Konzentrationen für ihre Messungen.