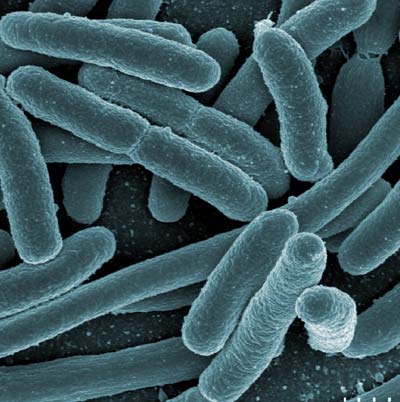
Vielfältig und resistent: Die Bakterien im Körper der Yanomami sind so artenreich wie bei keinem zuvor analysierten Menschen – ein Hinweis darauf, wie stark unsere westliche Lebensweise unsere mikrobiellen Mitbewohner verändert hat. Überraschend auch: Das isolierte Amazonasvolk trägt bakterielle Resistenzen selbst gegen modernste synthetische Antibiotika, obwohl sie nie in Kontakt mit der modernen Medizin waren, wie Forscher im Fachmagazin „Science Advances“ berichten.
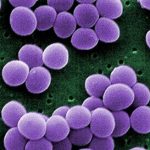
Jeder von uns trägt mehr Mikroben im Körper als eigene Zellen. Die meisten dieser Mitbewohner sind nicht nur harmlos, sie sind auch essenziell für unsere Gesundheit. Sie beeinflussen unser Immunsystem, helfen bei der Verdauung und beeinflussen vermutlich sogar, was wir essen. Auch für die Weitergabe von Resistenzen an Krankheitserreger spielt die Darmflora eine wichtige Rolle.
Isoliertes Amazonasvolk
Bei jedem von uns ist das Mikrobiom durch typische Einflüsse der Zivilisation wie industriell hergestellte Lebensmittel und die Einnahme von Antibiotika und anderen Medikamenten geprägt. „Aber wie stark sich das menschliche Mikrobiom durch unseren westlichen Lebensstil verändert hat, war bisher unbekannt“, erklären Jose Clemente von der Icahn School of Medicine am Mount Sinai Hospital in New York und seine Kollegen. Um das herauszufinden, haben sie nun erstmals das Mikrobiom der Yanomami analysiert.
Dieses erst in den 1960er Jahren entdeckte Volk lebt als Jäger und Sammler im Amazonasgebiet. In Venezuela existierten bis heute halbnomadische Gruppen der Yanomami, die von der modernen Zivilisation weitgehend isoliert sind. In einem dieser Dörfer nahmen die Forscher von 34 Bewohnern Speichel- und Kotproben und machten Hautabstriche, analysierten diese auf ihre Mikrobenzusammensetzung und verglichen diese Ergebnisse mit Analysen von Menschen aus den USA und von Amazonas-Stämmen mit intensivem Kontakt zu westlicher Lebensweise