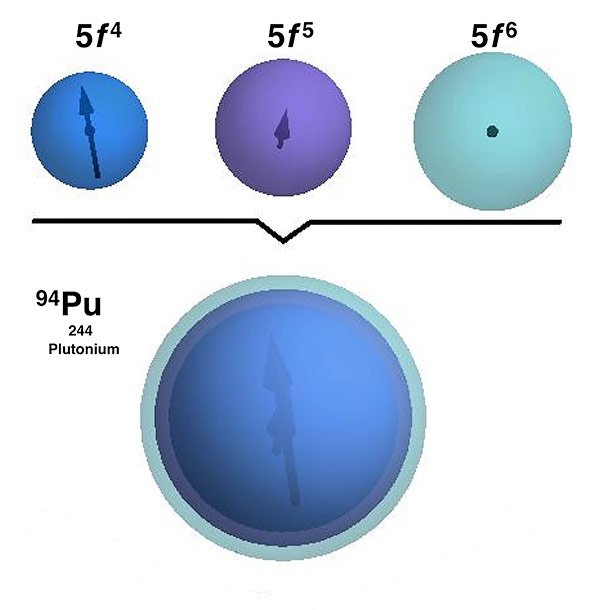
Seit Jahrzehnten rätseln Chemiker, warum Plutonium nicht magnetisch ist – obwohl es das der Theorie nach sein müsste. Jetzt haben Forscher eine Antwort gefunden: Die Elektronen des Plutoniums fluktuieren ständig zwischen drei Konfigurationen. Weil diese unterschiedlich magnetisch sind, reagiert das Element im Grundzustand wie ein Nichtmagnet. In Wirklichkeit aber besitze Plutonium einen dynamischen Magnetismus, so die Forscher im Fachmagazin „Science Advances“.
Plutonium ist eines der schwersten natürlich vorkommenden Elemente, das Actinoid mit der Ordnungszahl 94 ist zudem giftig und stark radioaktiv. Doch das ist nicht alles: „Plutonium ist zwar für die Instabilität seines Kerns bekannt, der die Kernspaltung ermöglicht“, erklären Marc Janoschek vom Los Alamos National Laboratory (LANL) und seine Kollegen. „Aber die Elektronenwolke um den Plutoniumkern ist genauso instabil.“
Zwischen den Stühlen
Schuld daran ist die spezielle Position von Plutonium im Periodensystem. Denn das Element sitzt unter den Actinoiden sozusagen zwischen den Stühlen. Links von ihm stehen mit Thorium, Palladium, Uran und Neptunium Atome, deren Elektronen des 5f-Orbitals delokalisiert sind. Wie für viele Metalle typisch, trägt dieser „Fermi-See“ aus Elektronen zur Bindung mit benachbarten Atomen im Gitter bei. „Im Gegensatz dazu sind die 5f-Elektronen der schwereren Actinoide lokalisiert, sie nehmen nicht an Bindungen teil“, so die Forscher.
Doch das Plutonium sitzt genau dazwischen. Seine 5f-Elektronen können daher je nach Temperatur und Zustand des Elements verschiedenste Verhaltensweise zeigen. „Das macht Plutonium zum elektronisch komplexesten Element des Periodensystems“, sagt Janoschek. „Für ein eigentlich simples Metall besitzt es verblüffend komplizierte Eigenschaften, die sich seit den 1940ern unserem Verständnis entziehen.“