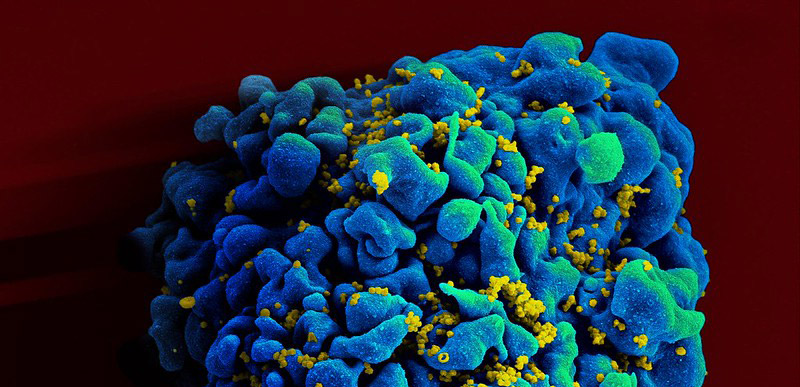
Hoffnung gegen Aids: Ein erster mRNA-Impfstoff gegen Aids hat sich in Versuchen mit Mäusen und Affen als vielversprechend erwiesen. Die Impfung mit den Gencodes zweier Virenproteine rief eine starke Antikörper-Antwort gegen gleich mehrere Varianten des HI-Virus hervor. Bei Makaken senkte eine mehrfache Impfung das Infektionsrisiko um 79 Prozent. Das weckt die Hoffnung, dass die gegen das Coronavirus erfolgreiche mRNA-Technologie auch im Kampf gegen HIV helfen könnte.
Während die Impfstoffentwicklung gegen das Coronavirus nicht einmal ein Jahr dauerte, suchen Forscher bei Aids schon seit 40 Jahren nach einer geeigneten Impfstrategie – bisher weitgehend vergeblich. Alle Versuche, das Immunsystem durch Lebendimpfstoffe, Protein-Impfstoffe oder genbasierte Vakzine gegen das HI-Virus zu wappnen, haben enttäuschende Ergebnisse erbracht. Der bisher beste Ansatz erreichte in klinischen Studien eine Schutzwirkung von nur rund 30 Prozent – und selbst das konnte nicht reproduziert werden.
Warum die Impfstoffentwicklung gegen HIV so schwierig ist
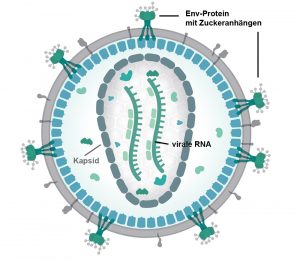
Das Problem: Das Hüllprotein (Env) des HI-Virus ist hochvariabel und verändert sich leicht. Zudem sind wichtige Erkennungsmerkmale der viralen Proteinhülle durch Zuckeranhänge verdeckt. Beim HI-Virus bilden diese Glykane einen fast flächendeckenden „Tarnmantel„. Die Folge: „Durch eine Impfung neutralisierende Antikörper zu erzeugen, hat sich als extrem schwierig erwiesen und selbst nach einer natürlichen Infektion bildet nur ein Bruchteil der Betroffenen solche Antikörper aus“, erklären Peng Zhang vom US National Institute of Allergy and Infectious Diseases (NIAID) und seine Kollegen.
Doch die mRNA-Technologie bietet nun neue Chancen, diese Probleme zu überwinden. Denn mit ihr lassen sich die Gencodes für bestimmte Virenproteine und Proteinteile in einem Vakzin vereinen und auf optimale Wirkung hin maßschneidern. „Unser experimenteller Impfstoff kombiniert gleich mehrere Merkmale, die die Defizite bisheriger HIV-Vakzinkandidaten ausgleichen“, erklärt Seniorautor Anthony Fauci vom NIAID.
Bauanleitungen zweier Virenproteine kombiniert
Konkret besteht der neue HIV-Impfstoff zum einen aus RNA mit der Bauanleitung des viralen Hüllproteins Env. In der für die ersten Impfdosen verabreichten Variante fehlen diesem Hüllprotein einige Zuckeranhänge, wodurch sie vom Immunsystem besser erkannt werden können. Das Vakzin für die Booster-Dosen enthält dagegen den Code für das vollständige Protein mehrerer HIV-1-Mutanten. „Dies soll die B-Zell-Antwort auf gemeinsame Antikörper-Ansatzstellen dieser Varianten stärken“, erklärt das Team.
Entscheidend auch: Das mRNA-Vakzin enthält den Gencode für ein zweites Virenprotein (Gag). Die Kombination dieser beide Proteine reicht aus, um im Körper die Bildung virenähnlicher Partikel anzuregen – kleiner Gebilde, deren Oberfläche der natürlicher HI-Viren ähnelt. In ersten Tests mit Mäusen führte dies dazu, dass alle geimpften Tiere neutralisierende Antikörper entwickelten, wie Zhang und seine Kollegen berichten.
Antikörper und T-Zellen gegen HIV
Wie gut dieses mRNA-Vakzin gegen eine HI-Infektion schützt, haben die Forscher mit 14 Makaken untersucht. Die Hälfte der Affen erhielt jeweils im Abstand von zwei bis drei Wochen eine Dosis der verschiedenen Impfstoffvarianten, die anderen blieben ungeimpft. Wie das Team feststellte, wurde der Impfstoff gut vertragen, die Tiere entwickelten nur eine vorübergehende Appetitlosigkeit.
Das Ergebnis: Schon nach der ersten Boosterdosis stiegen die Titer der neutralisierenden Antikörper bei den geimpften Affen deutlich an, fielen aber relativ zügig wieder ab. Erst nach der dritten Impfung blieben die Antikörper stabil auf hohem Niveau, wie Zhang und seine Kollegen berichten. Auch die zelluläre Immunantwort reagierte auf das Vakzin: Nach einem halben Jahr waren sowohl T-Killerzellen als auch T-Helferzellen gegen HIV nachweisbar, nach gut einem Jahr war ihre Aktivität durch die Boosterimpfungen noch einmal deutlich angestiegen.
Ansteckungsrisiko um 79 Prozent reduziert
Dann folgte der entscheidende Test: Gut ein Jahr nach der ersten Impfung bekamen alle Tiere einmal wöchentlich eine verdünnte Lösung von HI-Viren in den After gespritzt. Bei den ungeimpften Affen führte dies im Schnitt nach dem dritten Virenkontakt zu einer Infektion. „Im Gegensatz dazu zeigten zwei der sieben immunisierten Tiere auch nach 13 Wochen keinerlei Anzeichen für eine Infektion“, berichten die Wissenschaftler. Die restlichen fünf Affen infizierten sich erst mit erheblicher Verzögerung, im Schnitt erst nach dem achten Virenkontakt.
Die geimpften Tiere hatten demnach ein um 79 Prozent verringertes Risiko, sich bei einem ungeschützten Kontakt mit dem HI-Virus anzustecken. Dieser Immunschutz wirkte zudem gegen zwölf verschiedene Varianten des Erregers. „Eine solche mRNA-Plattform repräsentiert damit einen vielversprechenden Ansatz für die Entwicklung eines Impfstoffs gegen Aids“, konstatiert das Forschungsteam.
Weitere Optimierung nötig
Als nächsten Schritt planen die Wissenschaftler nun, den Vakzinkandidaten weiter zu optimieren, damit weniger Boosterimpfungen nötig sind. Denn ein Impfregime aus sieben oder mehr Dosen würde von Menschen kaum akzeptiert und wäre in vielen ärmeren Ländern auch schwer umzusetzen. „Wir passen unser Impf-Protokoll daher an, um die Qualität und Quantität der dadurch erzeugten virenähnlichen Partikel zu erhöhen“, erklärt Studienleiter Paolo Lusso vom NIAID.
Wenn sich dann auch die optimierten Vakzin-Varianten im Tierversuch als erfolgreich und sicher erweisen, soll eine erste klinische Studie der Phase 1 folgen. Dabei wird der Impfstoff zunächst gesunden Freiwilligen verabreicht, um die Verträglichkeit für de Menschen zu prüfen. (Nature Medicine, 2021; doi: 10.1038/s41591-021-01574-5)
Quelle: NIH/National Institute of Allergy and Infectious Diseases