Unter normalen Bedingungen können die Reparaturmechanismen der Zelle Schäden am Erbgut oder wichtigen Molekülen des Zellstoffwechsels ausgleichen. Mit steigendem Alter jedoch nimmt die Effektivität der Reparaturmechanismen ab. Als Folge mehren sich Fehlfunktionen, immer mehr Zellen entarten oder sterben ab. Diese Zellalterung bildet im Grunde die Basis des gesamten Phänomens der Alterung – ist also im Prinzip der völlig normale Lauf der Dinge.
Hirnschwund als unausweichliches Schicksal?
Auf einer Konferenz zu neurodegenerativen Erkrankungen im Herbst 2006 postulierte der Neurowissenschaftler Christian Haass von der Ludwig-Maximilians-Universität München dann auch provokant aber folgerichtig: Alle Menschen, so sie denn nur lange genug leben, erkranken an Alzheimer. Es sei nur eine Frage der Zeit bis sich genügend zerstörerische Eiweißablagerungen im Gehirn gebildet haben, um die Demenzerkrankung auszulösen.
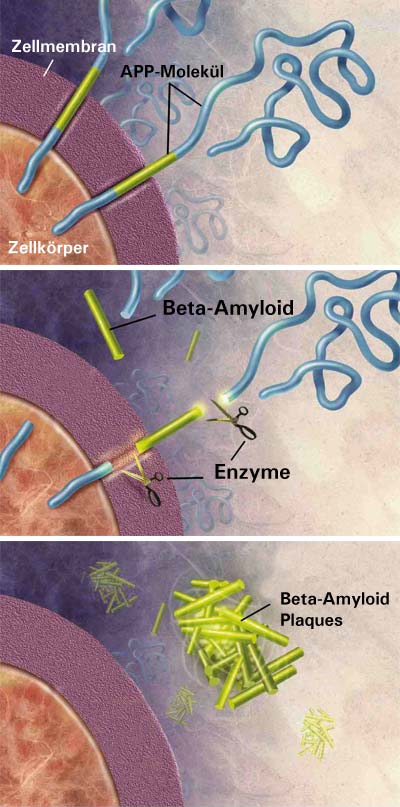
Haass hatte bereits 1992 gezeigt, dass die unlöslichen Eiweißbruchstücke, die sich im Gehirn von Alzheimer-Patienten als so genannte Plaques ablagern, auch bei Gesunden ein Leben lang im Gehirn entstehen. Die aus dem Protein Amyloid-Beta bestehenden Bruchstücke bilden sich, weil eine molekulare Schere, Beta-Secretase oder BACE1 genannt, sie aus dem Amyloid-Vorläuferprotein APP herausschneidet. Warum das geschieht, ist noch völlig unklar.
Auch hier sind Gene im Spiel
Anfang 2007 jedoch hat ein internationales Forscherteam immerhin ein neues Puzzleteil im Entstehungsrätsel der Plaques entdeckt: „Wissenschaftler haben bisher drei Gene identifiziert, deren Varianten ein frühes Einsetzen von Alzheimer auslösen können und eines, dass das Risiko für die späte Form erhöht,“ erklärt Richard J. Hodes, Leiter des National Institute für Aging der amerikanischen Gesundheitsbehörde NIH. „Wir verstehen zwar noch nicht völlig, was die Alzheimer-Krankheit verursacht, aber wir wissen, dass genetische Faktoren eine Rolle spielen können.”
Für die Studie hatten mehr als 6.000 Freiwillige Blut für eine Genanalyse gespendet. Die Forscher suchten dabei gezielt nach kleinen Veränderungen und Mutationen in sieben Genen. Diese kodieren eine Gruppe von Proteinen, die das APP innerhalb der Zellen transportieren. Bei der Untersuchung von Blutzellen lag die Konzentration eines dieser Proteine, SQRL1, bei Alzheimerpatienten um mehr als die Hälfte niedriger als bei Gesunden. In den Laborexperimenten riefen niedrige SQRL1-Konzentrationen tatsächlich eine höhere Produktion von Amyloid-Beta-Bruchstücken hervor.
Stand: 26.10.2007