Rund 90 Prozent der Menschen tragen es in sich: das Humane Herpesvirus 1. Doch die wenigsten von uns merken etwas davon, da die Infektion mit diesem Erreger meist völlig ohne Symptome verläuft. Virus und Wirt leben quasi symbiotisch miteinander – zumindest solange das Immunsystem des Wirts intakt ist.
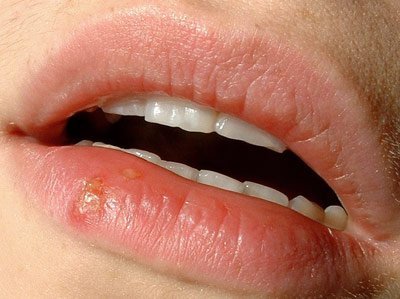
Herpesbläschen an der Lippe © gemeinfrei
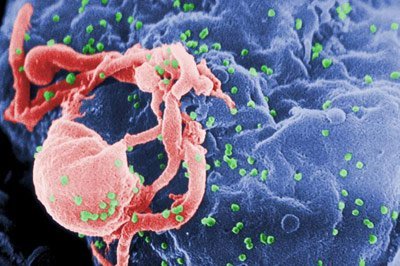
Während aggressive, akute Viren wie Influenza, Ebola oder Aids sich in ihren Wirten rapide vermehren, Zellen und Gewebe zerstören und im schlimmsten Fall den Tod verursachen, verhält sich das Herpes-Virus anders. Es vermehrt sich nicht mehr ungezügelt und seine krankmachende Wirkung ist nur noch minimal. Erst wenn unsere Immunabwehr durch Stress oder Krankheit geschwächt ist, ändert sich dies und der „Eindringling“ macht sich durch Lippenbläschen oder Ekzeme bemerkbar.
„Viren haben mehr als eine Überlebens-Strategie: Nicht alle Viren sind sich rapide vermehrende, schnell verändernde Erreger von Krankheiten“, erklärt Luis Villarreal, Leiter des Center for Virus Research an der Universität von Kalifornien in Irvine. Stattdessen verbindet Mensch und Virus im Falle des Herpesvirus, wie auch bei anderen persistenten Viren, eine lange, vermutlich sogar Jahrmillionen dauernde gemeinsame Geschichte. In ihrem Verlauf wandelte sich der Erreger von einem akuten, seinen Wirt tötenden Parasiten zu einem symbiotischen Mitbewohner.
Echte Symbiose statt „Wettrüsten“?
So lautet jedenfalls die provozierende Theorie von Villarreal und einigen anderen Virenforschern. Wie der bekannte britische Wissenschaftsautor, Arzt und Evolutionsbiologe Frank Ryan in seinem neuen Buch „Virolution“ darlegt, widerspricht diese Sicht des symbiotischen Miteinanders von Mensch und Virus diametral den herkömmlichen Vorstellungen eines „Gleichgewichts des Schreckens“, der prekären Koexistenz auf Basis beiderseitiger Aufrüstungsmaßnahmen.
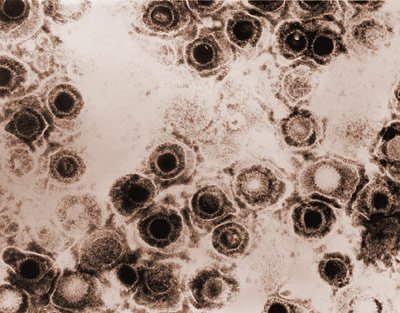
Herpes simplex- Viren bleiben, einmal eingedrungen, ein Leben lang in uns. © CDC
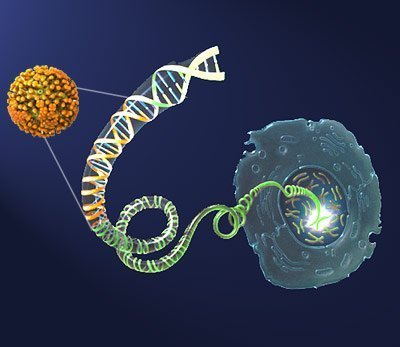
Denn per Definition ist eine Symbiose eine Partnerschaft, bei der jede Seite von der Anwesenheit der anderen profitiert. Jeder Partner steuert eine Fähigkeit oder Eigenschaft bei, die dem anderen fehlt und ihm daher nützlich ist. „Was der Wirt im Falle einer Wirt-Virus-Beziehung beiträgt, liegt auf der Hand: Er bietet dem Virus Obdach und stellt seine genetische Maschinerie zur Verfügung, so dass das Virus Kopien seiner selbst anfertigen kann“, erklärt Ryan. Aber was steuert das Virus bei?
Der Feind meines Feindes ist mein Freund
Den entscheidenden Hinweis darauf brachten unter anderem Beobachtungen an Affen. Auch bei diesen gibt es Herpesviren, die extrem eng an jeweils eine Affenart angepasst sind und bei diesen keinerlei Krankheitssymptome auslösen. „Wenn man sie mit einer anderen Affenart in Kontakt bringt, wirken sie äußerst, wirklich äußerst letal“, erklärt Max Essex, Professor für Medizin an der Harvard Universität, in Ryans Buch.
„Ich vermute, man könnte sogar nachweisen, dass genau jene Affen am empfindlichsten auf das jeweilige Virus reagieren, die dieselbe ökologische Nische besetzen und zum Beispiel dieselbe Nahrung bevorzugen, während andere Arten, die vielleicht im selben Revier leben aber etwas anderes fressen und somit eine andere Nische ausfüllen, nicht so leicht erkranken.“
Mit anderen Worten: Der Träger eines persistenten Virus profitiert, weil sein Mitbewohner ihm auf sehr effektive Weise unliebsame Konkurrenz aus dem Weg räumt. Oder, wie es Ryan formuliert: „Bei Licht besehen haben auch Viren eine wichtige, wenngleich weniger augenfällige Fähigkeit, die ihren Wirten fehlt: Ihnen wohnt ein immenses Vernichtungspotenzial inne.“

Parapox-Viren helfen dem Grauhörnchen gegen den Konkurrenten, das Eichhörnchen. © Ray eye/CC-by-sa 2.0, gemeinfrei
Virus hilft Grauhörnchen gegen Konkurrent
Wie gut das Beseitigen von Konkurrenz als Gegenleistung des Virus für seinen Wirt funktioniert, zeigt ein Beispiel aus England: Hier breitet sich seit Jahren das aus Amerika eingeschleppte Grauhörnchen (Sciurus carolinensis) immer weiter aus und bedroht inzwischen sogar den Fortbestand des heimischen Roten Eichhörnchens (Sciurus vulgaris).
Lange Zeit hielt man den Einwanderer wegen seiner Größe und Aggressivität für so erfolgreich, doch inzwischen musste man sich eines Besseren belehren lassen, wie Ryan erzählt: „Inzwischen hat sich herausgestellt, dass die Grauhörnchen-Population mit einem Parapoxvirus durchseucht ist, das bei seinem Symbiosepartner keine Krankheitssymptome hervorruft, für das Europäische Eichhörnchen aber tödlich ist.“ Um der grassierenden Parapocken-Übertragung Einhalt zu gewähren, werden seit 2007 in Schottland regelmäßig Grauhörnchen getötet.
Nadja Podbregar
Stand: 05.11.2010