Trotz der großen Fortschritte ist die Stammzellforschung und -medizin noch immer vor allem eines: Grundlagenforschung. Denn noch immer sind zu viele Aspekte der komplexen Physiologie und Genetik der Stammzellen und der Prozesse, die bei der Reprogrammierung ablaufen ungeklärt. Das zeigte sich zuletzt im Jahr 2011. Damals schreckte eine ziemlich schlechte Nachricht die Gemeinschaft der Stammzellforscher auf: Ein internationales Forscherteam entdeckte zahlreiche Hinweise darauf, dass in Kultur gehaltene Stammzellen sich im Laufe der Zeit verändern – und dies nicht zum Guten.
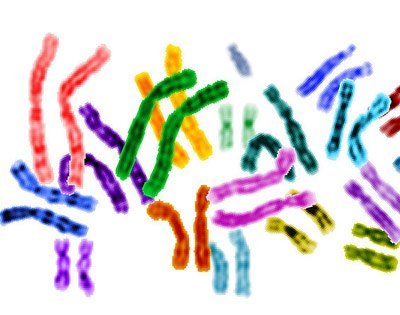
Überschüssige Kopien und fehlende Gene
Bei der Genanalyse von jeweils mehr als hundert Proben aus embryonalen und induzierten Stammzelllinien stießen die Wissenschaftler auf zahlreiche schwerwiegende Veränderungen im Erbgut der Zellen. Vor allem bei den embryonalen Stammzellen lagen einige DNA-Abschnitte in ungewöhnlich hoher Kopienzahl vor. Bei den durch Reprogrammierung erzeugten Stammzellen waren mehrere Tumorsuppressor-Gene verschwunden. Diese Gene sorgen normalerweise dafür, dass potenzielle Krebsgene abgeschaltet bleiben und die Zelle dadurch nicht entartet. Fehlen sie, kann dies zu Krebs führen. „Unsere Ergebnisse zeigen, dass genetische Abnormitäten bei pluripotenten Stammzellen entstehen können“, konstatieren die Forscher um Louise Laurent von der University of California in San Diego.
Brisant machte die Studie auch die Erkenntnis, dass die festgestellten genetischen Aberrationen mit den gängigen Testmethoden nicht gefunden werden. Denn normalerweise prüfen Forscher die Qualität ihrer Stammzellkulturen vor allem visuell: Sie fertigen Präparate an, auf denen die Chromosomen komplett zu sehen sind – das sogenannte Karyotyping – um mögliche Brüche der Erbgutpakete oder fehlende Chromosomen zu erkennen. Zudem wird das Aussehen der Zellen und ihr Teilungsverhalten mit Hilfe von Mikroskopen beobachtet. Doch genau dies reicht nicht aus, wie Laurent und ihre Kollegen betonen. „Die meisten der Genveränderungen können durch Karyotying oder Mikroskop-basierte Methoden nicht detektiert werden“, konstatieren sie. „Es ist daher dringend nötig, diese Zellkulturen häufig genetisch zu untersuchen, um ihre Stabilität und Sicherheit zu gewährleisten.“
Krebs nach Stammzellen-Therapie
Ganz überraschend kam die Entdeckung dieser genetischen Aberrationen allerdings nicht: Bereits in den Jahren davor waren vereinzelt Krebsfälle bei Patienten aufgetreten, die im Rahmen klinischer Studien mit Stammzellen behandelt worden waren. 2009 dann berichteten israelische Forscher über einen Fall, bei dem sich aus transplantierten neuralen Stammzellen Hirntumoren entwickelt hatten. Ein neunjähriger Junge war seit Mai 2001 mehrmals mit Stammzellen behandelt worden, um seine unheilbare Erbkrankheit, die sogenannte Ataxia telangiectasia, zu lindern. Diese geht mit fortschreitenden Hirnschädigungen einher, die durch Gabe der neuralen Stammzellen ausgeglichen werden sollten.
Doch vier Jahre nach Beginn der Injektionen bildeten sich im Gehirn und Rückenmark des Jungen mehrere, langsam wachsende Tumore. Dass diese durch die transplantierten Zellen ausgelöst worden waren, belegte die molekularbiologische Analyse: In den Tumorproben fanden sich sowohl männliche als auch weibliche Zellen, zudem trug keine von ihnen den Gendefekt der Ataxia telangiectasia. Beides ein klares Indiz dafür, dass die entarteten Zellen ihren Ursprung in den von zwei Spendern stammenden neuralen Stammzellen hatten.
„Diese Beobachtung ist ohne Zweifel ein Rückschlag für die Entwicklung zellbasierter Therapien mit neuralen Stammzellen zur Korrektur definierter genetischer Defekte“, erklärte damals der Neurologe Michael Weller, ehemaliger Sprecher der Neuroonkologischen Arbeitsgemeinschaft (NOA) in er Deutschen Krebsgesellschaft.
Nadja Podbregar
Stand: 13.09.2013