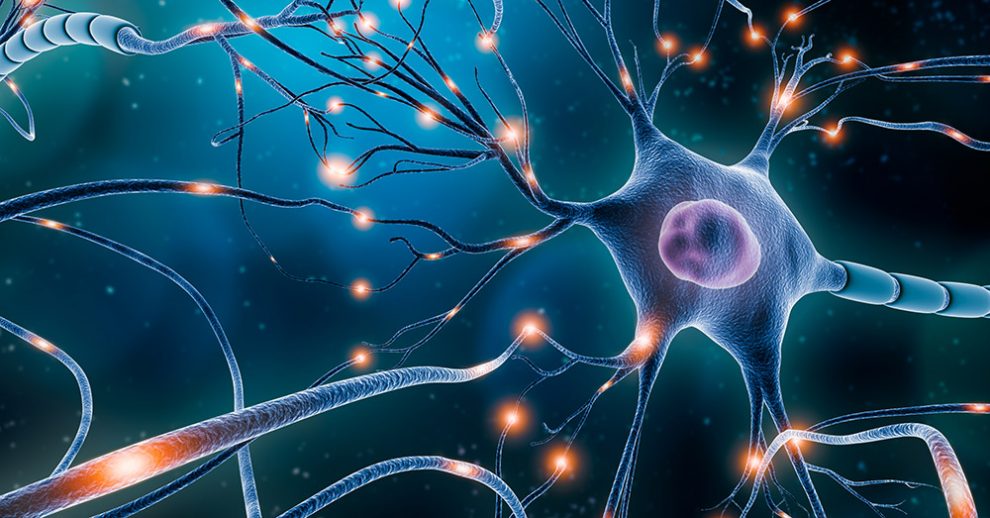
Angriff von innen: In unserem Erbgut gibt es Reste alter Viren, die die Gehirnentwicklung massiv beeinträchtigen können – und dadurch beispielsweise neurologische Krankheiten mitverursachen. Den Effekt eines dieser endogenen Retroviren haben Forschende jetzt im Experiment beobachtet. Demnach trägt seine Aktivierung zur Entstehung fehlgebildeter und funktionsloser Neuronen in der Großhirnrinde bei und stört die Schichtbildung des heranwachsenden Gehirns.
Viren befallen uns nicht nur von außen, wir tragen sie auch in unserem Erbgut: Rund acht Prozent unserer DNA besteht aus endogenen Retroviren (HERV) und weitere rund 35 Prozent entfallen auf kleinere Fragmente viralen Ursprungs. Sie sind größtenteils über Infektionen unserer fernen Vorfahren ins Genom gelangt, aber es gibt auch heutige Erreger wie das Coronavirus SARS-CoV-2, die genetische Spuren im Erbgut infizierter Zellen hinterlassen können. In der Regel verlieren diese endogenen Viruselemente ihre Fähigkeit zur Replikation und Infektion.
Helfer und Krankmacher zugleich
Doch inaktiv sind die HERVs deswegen nicht. Schon länger gibt es Hinweise darauf, dass einige endogene Retroviren von unserer Zellmaschinerie abgelesen und aktiviert werden – und dadurch positive wie negative Effekte bewirken. So scheint eines dieser viralen Elemente den Schutz vor Krebs zu verstärken, ein anderes fördert das Muskelwachstum bei Männern. Andererseits stehen einige HERVs schon länger im Verdacht, an neurologischen Erkrankungen wie der Multiplen Sklerose, ALS oder der Creutzfeld-Jacob-Krankheit mitbeteiligt zu sein.
Welche konkreten Auswirkungen reaktivierte HERVs auf das Gehirn haben können, enthüllt nun das Experiment eines Forschungsteams unter Leitung von Michelle Vincendeau vom Helmholtz Zentrum München. Dafür hatten die Forschenden mithilfe des Genwerkzeugs CRISPR gezielt eine spezielle Gruppe von endogenen Retroviren im Genom von neuronalen Stammzellen aktiviert. „Die HERV-K (HML-2) wurden mit neurotoxischen Wirkungen in Verbindung gebracht, aber man wusste bisher nicht, welche Rolle sie dabei spielen oder wie sie wirken“, erklärt das Team.
HERV fördert Fehlbildung von Neuronen
Es zeigte sich: Werden diese endogenen Retroviren aktiviert, löst dies eine Kaskade der Aktivierung weiterer Gene aus, die die Entwicklung der neuronalen Stammzellen zu Nervenzellen beeinflussen und die Hirnentwicklung stören. Bei der Ausreifung von Neuronen der Großhirnrinde bildeten sich dadurch fehlgebildete und funktionsunfähige Zellen mit anomal kurzen und kaum verzweigten Zellfortsätzen, wie die Forschenden beobachteten.
„Wir haben festgestellt, dass eine erhöhte Transkription von HERV-K(HML-2) schädlich für die Entwicklung und Funktion der kortikalen Neuronen ist“, berichten Vincendeau und ihre Kollegen. Dabei scheinen diesen Effekte stark vom Neuronentyp abzuhängen. Denn spezielle Neuronen, die den Hirnbotenstoff Dopamin herstellen, waren offenbar nicht von der Aktivierung der endogenen Retroviren beeinträchtigt, wie die Versuche ergaben.
In ergänzenden Tests stellte das Team zudem fest, dass die Aktivierung dieser HERVs auch die Ausbildung der Hirnstruktur stört: Im Labor gezüchtete Miniversionen des Vorderhirns entwickelten unter Einfluss der aktivierten endogenen Retroviren eine veränderte Schichtstruktur.
Wenn die Kontrolle versagt
Die Ergebnisse bestätigen den Verdacht, dass zumindest einige endogene Retroviren an neurologischen Krankheiten und Fehlbildungen beteiligt sein könnten. Allerdings: Unter normalen Umständen verhindern Anlagerungen an der DNA die Aktivierung dieser und anderer endogener Retroviren. Diese epigenetischen Anhänge blockieren das Ablesen dieser DNA-Abschnitte und halten damit die Virenelemente unter Kontrolle – jedenfalls bei der normalen Hirnentwicklung.
Bei bestimmten neurodegenerativen Erkrankungen könnten diese Kontrollmechanismen aber versagen und so zu einer Aktivierung der HERVs führen, wie das Forschungsteam erklärt. Es ist bereits bekannt, dass Umweltfaktoren wie Viren, Bakterien und UV-Licht verschiedene HERVs aktivieren können und damit möglicherweise zum Ausbruch von Krankheiten beitragen.
Neuer Ansatzpunkt für Therapien?
Das Wissen darüber, welche dieser HERVS bei welchen neurologischen Krankheiten aktiv sind, könnte daher neue Ansätze für eine Behandlung oder Prävention eröffnen, so die Hoffnung von Vincendeau und ihrem Team. In einem nächsten Schritt planen die Forschenden deshalb, den umgekehrten Weg näher zu erforschen: die gezielte Deaktivierung von endogenen Retroviren in Proben von Neuronen erkrankter Personen. (Cell Stem Cell, 2021; doi: 10.1016/j.stem.2021.04.009)
Quelle: Helmholtz Zentrum München