Neue Hoffnung gegen Thrombosen und Gerinnungsstörungen: Ein Protein auf der Oberfläche unserer Blutplättchen spielt eine zuvor unerkannte Rolle bei der Blutgerinnung, wie Forschende entdeckt haben. Dieses Glykoprotein V reguliert die Bildung von verklebenden Fibrinfasern im Blut – und verhindert so eine übermäßige Gerinnselbildung. Dies eröffnet neue Möglichkeiten, die Blutgerinnung zu kontrollieren, ohne dass das Blut „zu dünn“ wird. Dies könnte Thrombosen, Schlaganfällen und Herzinfarkten vorbeugen.
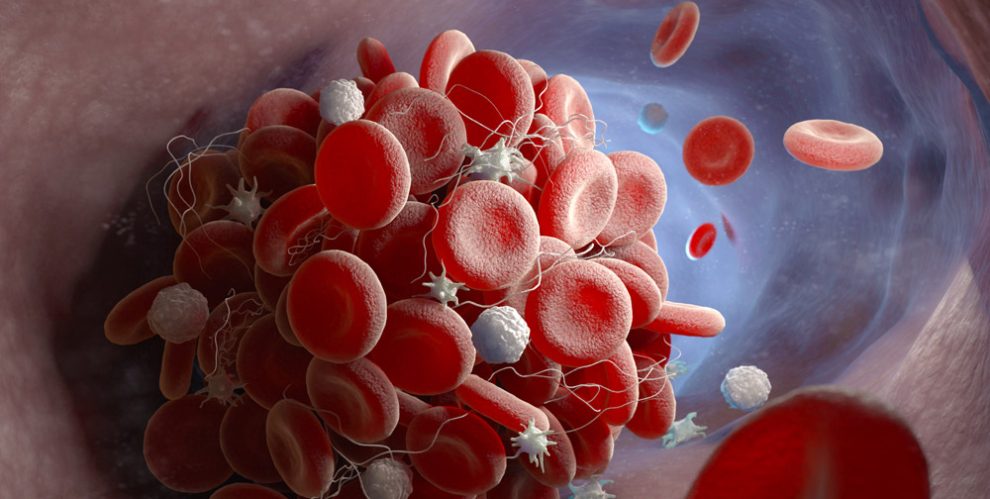
Eine funktionierende Blutgerinnung – fachsprachlich Hämostase – ist für uns überlebenswichtig. Ohne sie würden wir schon durch kleine Verletzungen verbluten. Entscheidend dafür sind zwei Vorgänge: Bei der Blutstillung heften sich Blutplättchen an die Wundränder, bilden einen Pfropf und dichten die Verletzung provisorisch ab. Die Blutgerinnung sorgt dann dafür, dass lange Fasern aus Fibrin gebildet werden, die mit den Blutplättchen verklumpen und so die Wunde fest abdichten.
Doch bisher war erst in Teilen geklärt, wie diese Fibrinbildung reguliert wird. Denn wenn zu viele Fibrinfasern gebildet werden, kann es zu Thrombosen, Gefäßverschlüssen und im schlimmsten Fall zu Schlaganfall und Herzinfarkt kommen.
Blutplättchen-Protein im Visier
Jetzt haben Forschende um Sarah Beck vom Universitätsklinikum Würzburg den entscheidenden Akteur dieses blutungsstillenden Prozesses entdeckt. Für ihre Studie hatten sie die Funktion des sogenannten Glykoproteins V (GPV) untersucht, einem Rezeptor auf der Oberfläche der Blutplättchen. Bekannt war bereits, dass dieses Protein durch das Enzym Thrombin zerteilt werden kann, dass für die Bildung der Fibrinfasern verantwortlich ist. Unklar war jedoch, wozu diese Spaltung des GPV dient und ob sie eine Rolle bei der Blutgerinnung spielt.
Um mehr darüber zu erfahren, führten Beck und ihr Team Versuche mit Mäusen durch, bei denen das GPV so mutiert war, dass es nicht mehr durch Thrombin aufgespalten werden konnte. Dies hatte eine überraschende Folge: „Von uns unerwartet zeigten diese Mäuse eine beschleunigte Thrombusbildung bei arteriellen Verletzungen“, berichtet das Team. Weil das abgespaltene, gelöste GPV im Blut fehlte, kam es zu einer übermäßigen Synthese der gerinnungsfördernden Fibrinfasern.
GPV verhindert gefährliche Gerinnsel
Damit ist klar: Das GPV-Protein spielt eine bisher unerkannte Rolle bei der Blutgerinnung. „Damit konnten wir erstmals eine neue Schaltstelle aufdecken, die sowohl die Blutstillung als auch die Bildung von Thrombosen reguliert“, sagt Seniorautor Bernhard Nieswandt von der Universität Würzburg. „GPV kontrolliert die Aktivität des Enzyms Thrombin, das für die Bildung von Fibrin verantwortlich ist.“
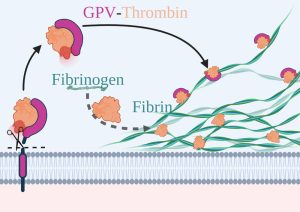
Nähere Analysen enthüllten auch, wie das GPV die überschießende Fibrinbildung reguliert: Das vom Thrombin von der Oberfläche der Blutplättchen abgespaltene GPV bleibt ans Thrombin gebunden und stört dadurch dessen Anlagerung an eine wachsende Fibrinfaser. Dies behindert die weitere Synthese – und hemmt damit auch die übermäßige Entstehung von gefährlichen Blutgerinnseln. In Versuchen mit Mäusen gelang es dem Forschungsteam, künstlich ausgelöste Schlaganfälle durch gezielte Gabe von gelöstem GPV zu verhindern. Auch andere Formen der Thrombusbildung ließen sich durch dieses Protein verhindern.
Hilfe gegen Thrombosen, aber auch für Bluter
Nach Ansicht der Wissenschaftler eröffnen diese Erkenntnisse neue Möglichkeiten, Thrombosen und damit Schlaganfällen und Herzinfarkten vorzubeugen. Denn die bisher verfügbaren Wirkstoffe hemmen zwar die Bildung von Blutgerinnseln, stören aber auch die normale, für die Wundheilung wichtige Blutgerinnung. Der Einsatz von gelöstem GPV könnte nun dieses Problem umgehen, weil nur die übermäßige Fibrinbildung gehemmt wird, nicht aber der Rest der Gerinnungskaskade. „Die Prävention von Thrombosen bei gleichzeitiger Beibehaltung der Blutstillung ist schon lange ein zentrales Ziel der Forschung zu Antithrombosemitteln“, erklärt das Team.
Umgekehrt könnte die neu entdeckte Kontrollfunktion des GPV auch die Behandlung von Gerinnungsstörungen bei Blutern verbessern, beispielsweise indem die GPV-Spaltung durch Antikörper blockiert wird. „In einem experimentellen Modell zur Blutstillung konnte unser neuer Antikörper tatsächlich die Hämostase unter Bedingungen wiederherstellen, unter denen ansonsten keine Blutstillung möglich ist“, berichtet Beck. Auch hier biete das GPV großes Potenzial für neue Therapien. (Nature Cardiovascular Research, 2023; doi: 10.1038/s44161-023-00254-6)
Quelle: Universitätsklinikum Würzburg