Ein Protein macht den Anfang: Forscher haben herausgefunden, womit die Herz-Bildung im menschlichen Embryo beginnt. Demnach muss ein bestimmtes Protein in den noch undifferenzierten Stammzellen präsent sein, um den entscheidenden Schalter umzulegen. Dieses Protein beeinflusst, welche RNA-Bauanleitungen von den Ribosomen – den zellulären Proteinfabriken – bevorzugt ausgelesen werden. Auf diese Weise werden schon die frühen Zellen auf ihre Entwicklung zum Herzen programmiert.
Das Herz ist der Motor unseres Körpers, ohne diese Pumpe können wir nicht überleben. Deshalb ist das Herz auch das erste Organ, das im menschlichen Embryo angelegt wird. Schon rund drei Wochen nach der Befruchtung bereiten sich die ersten embryonalen Stammzellen darauf vor, einmal zu einem Herzen zu werden. Sie bilden einen Zellhaufen, in dem sich nach und nach die verschiedenen Zelltypen des Herzens ausdifferenzieren. Auch die Hohlräume für die Herzkammern entstehen. Etwa ab der fünften Woche beginnt das Herz des Embryos zu schlagen.
Was den Entwicklungsweg zum Herzen anstößt und welche Faktoren im Embryo dafür sorgen, dass die embryonalen Stammzellen das korrekte Programm anschalten, war jedoch unbekannt.
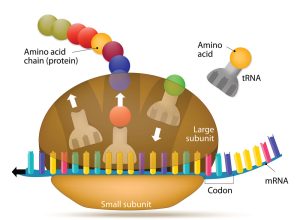
Ribosomen im Visier
Diesen „Anschalter“ für die Herzentwicklung haben nun Deniz Bartsch von der Universität Köln und seine Kollegen gefunden. Sie waren einer Spur nachgegangen, die sie zu den Ribosomen – den Proteinfabriken – der embryonalen Zellen führte. Dort beeinflussen an die Ribosomen angelagerte Proteine, welche von der Boten-RNA kodierten Bauanleitungen bevorzugt abgelesen und in Proteine umgesetzt werden. Dadurch können diese Ribosomen-assoziierten Proteine (RAP) die Entwicklung der Zelle entscheidend mitbeeinflussen.