Gestörte Funktion: Stark übergewichtige Menschen haben nicht nur einen veränderten Stoffwechsel, auch ihre Mitochondrien arbeiten weniger effektiv, wie eine Studie mit Mäusen enthüllt. Demnach fragmentiert eine kalorienreiche Ernährung die Mitochondrien und verringert so ihre Fettverbrennungskapazität – das fördert schon auf Zellebene das Zunehmen. Unterdrückten die Forschenden jedoch das dafür verantwortliche Gen in den Fettzellen, nahmen die Mäuse trotz fettreicher Ernährung nicht übermäßig zu.
Fettleibigkeit erhöht das Risiko für zahlreiche Krankheiten, darunter Herz-Kreislauf-Erkrankungen, Typ-2-Diabetes und Demenz. Doch gerade adipösen Menschen fällt das Abnehmen oft schwer. Studien haben gezeigt, dass Sport bei stark übergewichtigen Personen weniger effektiv ist, da der Körper den erhöhten Energieverbrauch durch Einsparungen beim Grundumsatz ausgleicht.
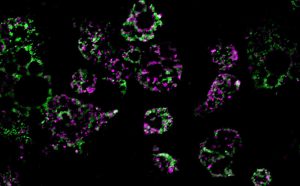
Diese Fluoreszenzaufnahme zeigt Mitochondrien in den Fettzellen von Mäusen. © UC San Diego
Verringerte Fettverbrennung durch fragmentierte Mitochondrien
Ein Team um Wenmin Xia von der University of California in San Diego hat nun einen weiteren Mechanismus entdeckt, der für eine verringerte Fettverbrennung bei Übergewichtigen sorgt. Um die Auswirkungen von Adipositas auf den Energiehaushalt des Körpers besser zu verstehen, fütterten die Forschenden Mäuse mit einer fettreichen Diät. Als die Tiere dadurch wie erwartet fettleibig geworden waren, untersuchte das Team die Prozesse in ihren Zellen.
„Die Fütterung mit einer fettreichen Diät führte bei den Mäusen dazu, dass sich die Mitochondrien in ihren Fettzellen fragmentieren“, berichten die Forschenden. „Dadurch verringerte sich ihre Kapazität zur Fettverbrennung.“ Große, effektive Mitochondrien zerfielen dabei in mehrere kleine, die das Fett nur unzureichend verarbeiten und in Energie umsetzen konnten. Dadurch verschlimmert sich die Fettleibigkeit weiter, wie Xia und seine Kollegen berichten.
Verantwortliches Gen identifiziert
Doch wie kommt es zu dieser ungewollten Kaskade? Bei näheren Analysen entdeckten Xia und sein Team, dass ein Protein namens RalA diesen schädlichen Prozess steuert. Schalteten die Forschenden das Gen für dieses Protein in den Fettzellen von Mäusen aus, behielten die Mitochondrien ihre effektive Form. Selbst bei einer sehr kalorienreichen Fütterung nahmen diese Mäuse dadurch nicht übermäßig zu.
„Das von uns identifizierte Gen ist ein entscheidender Bestandteil dieses Übergangs von gesundem Gewicht zu Fettleibigkeit“, sagt Xias Kollege Alan Saltiel. Bekannt ist, dass das RalA-Gen im Körper vielfältige Funktionen erfüllt. Unter anderem sorgt es dafür, dass defekte Mitochondrien abgebaut werden. Bei adipösen Mäusen – und wahrscheinlich auch Menschen – ist es allerdings überaktiv, wie das Team nun herausgefunden hat.
„Die chronische Aktivierung von RaIA scheint eine entscheidende Rolle dabei zu spielen, den Energieverbrauch in den Fettzellen Übergewichtiger zu unterdrücken“, erklärt Saltiel. „Wenn wir diesen Mechanismus verstehen, sind wir der Entwicklung gezielter Therapien, die Gewichtszunahme und damit verbundene Stoffwechselstörungen durch eine Steigerung der Fettverbrennung bekämpfen könnten, einen Schritt nähergekommen.“
Neuer Ansatz für Therapien?
Nach Angaben des Teams spricht einiges dafür, dass der jetzt bei Mäusen entdeckte Mechanismus auch beim Menschen abläuft: Einige der Proteine, die bei Mäusen von RalA beeinflusst werden, ähneln Proteinen beim Menschen, die bereits früher mit Fettleibigkeit und Insulinresistenz in Verbindung gebracht wurden. „Der direkte Vergleich zwischen der von uns entdeckten grundlegenden Biologie und den realen klinischen Ergebnissen unterstreicht die Relevanz der Ergebnisse für den Menschen und deutet darauf hin, dass wir in der Lage sein könnten, Fettleibigkeit zu behandeln oder zu verhindern, indem wir mit neuen Therapien auf den RaIA-Stoffwechselweg abzielen“, sagt Saltiel.
Da RalA auch bei einigen Krebsarten eine Rolle spielt, gibt es bereits Medikamente, die seine Aktivität hemmen. „RalA erweist sich deshalb als ein attraktives Ziel, um zu testen, wie sich der systemische Stoffwechsel bei Fettleibigkeit verbessern lässt“, schreiben Ludovica Zambello und Luca Scorrano von der Universität Padua in Italien in einem begleitenden Kommentar zur Studie. „Obwohl weitere Forschungen erforderlich sind, um den Mechanismus umfassend zu entschlüsseln, stellt diese Studie einen bedeutenden Fortschritt dar.“ (Nature Metabolism, 2024, doi: 10.1038/s42255-024-00978-0)
Quelle: University of California – San Diego