Beraubtes Eisen: Chemiker haben einen neuen, extrem elektronenarmen Zustand des Eisens erzeugt. In dieser Verbindung hat das Metallatom sieben Elektronen zu wenig und daher Oxidationsstufe VII – ein für Eisen nie zuvor nachgewiesener Zustand. Zwar ist der super-oxidierte Eisenzustand sehr kurzlebig, er liefert aber wertvolle Einblicke in die Reaktionschemie dieses biologisch und geologisch wichtigen Metalls, wie das Team in „Nature Chemistry“ berichtet. Auch neue Anwendungen könnten sich daraus ergeben.
Eisen ist eines der häufigsten Elemente auf der Erde und im gesamten Universum. Es spielt eine Schlüsselrolle für viele biochemische Prozesse in unserem Körper, darunter den Sauerstofftransport durch das Hämoglobin der Roten Blutkörperchen. Gleichzeitig ist Eisen auch in geochemischen Kreisläufen und als Rohstoff für Stahl ein wichtiges Element. Seine prominente Rolle verdankt das Metall vor allem seiner Fähigkeit, Redoxreaktionen anzustoßen und zu katalysieren. Selbst besonders stabile chemische Bindungen wie die Dreierbindung des Luftstickstoffs N2 kann Eisen aufspalten.
Elektronenklau beim Eisenatom
Wie gut Eisen chemische Bindungen aufbrechen und andere Elemente an sich ziehen kann, hängt von seiner Oxidationsstufe ab: Je mehr Elektronen das Eisen verliert, desto höher oxidiert und reaktiver wird es. „Aber nur eine Handvoll chemischer Verbindungen mit Eisen im hoch-oxidierten Zustand sind bisher bekannt“, erklären Martin Keilwerth von der Universität Erlangen-Nürnberg und seine Kollegen. Darunter sind nur zwei Verbindungen mit der bisher höchsten Oxidationstufe des Eisens, Eisen(VI). In ihr fehlen dem Metallatom sechs seiner Elektronen.
Doch Keilwerth und seinem Team ist es nun erstmals gelungen, dem Eisenatom auch noch ein siebtes Elektron zu entreißen. Für ihr Experiment erzeugten sie zunächst eine organische Komplexverbindung, in der ein Eisenatom mit Fluor und mehreren stickstoffhaltigen Kohlenwasserstoffringen assoziiert ist. In diesem Komplex hat das Eisenatom die Oxidationsstufe VI – schon das ist eine Seltenheit. Im nächsten Schritt ließen die Chemiker diesen sechswertigen Eisenkomplex mit einem starken, fluorhaltigen Oxidationsmittel reagieren.
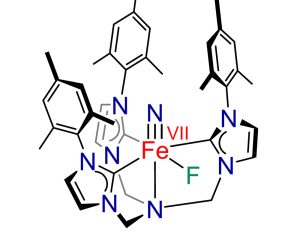
Erster Nachweis einer Oxidationsstufe VII beim Eisen
„Für uns unerwartet lässt sich der stabile Eisen(VI)-Komplex sogar noch weiter oxidieren“, berichten die Chemiker. Durch diese Reaktion entstand eine neuartige Komplexverbindung, in der das Eisen die Oxidationsstufe VII einnahm. „Das bedeutet, wir haben einem Eisenatom sieben Elektronen entfernt“, erklärt Koautor Dominik Munz von der Universität des Saarlandes. Zum ersten Mal ist es den Chemikern damit gelungen, Eisen in diesen extrem elektronenarmen Zustand zu bringen.
Das neuartige heptavalente Eisen ist so reaktionsfreudig, dass es nur bei extrem tiefen Temperaturen unterhalb von minus 50 Grad überhaupt stabil bleibt. Sobald die super-oxidierte Komplexverbindung erwärmt wird, bildet sie durch intramolekulare Umlagerungen eine neue, nur noch fünfwertige Eisenverbindung, einen zyklischen Eisen(V)-Imido-Komplex, wie das Team berichtet.
Wozu ist das gut?
Noch muss der neuentdeckte Eisenzustand weiter erforscht werden – auch was seine möglichen Anwendungen angeht. Grundsätzlich spielen solche hochoxidierten Verbindungen jedoch auf vielen praktischen Feldern eine Schlüsselrolle, besonders in der nachhaltigen Energiewirtschaft.
„In der Oxidationschemie, zum Beispiel zur Herstellung von Alkohol, könnte man sich einen Einsatz gut vorstellen, auch in der Batterietechnik, der Herstellung synthetischer Kraftstoffe und bei der Wasserspaltung“, erläutert Munz. Bisher dient das teure und seltene Element Iridium häufig als Katalysator für die Wasserspaltung, könnte man dieses jedoch durch hochoxidiertes Eisen ersetzen, wäre dies ein wichtiger Durchbruch. (Nature Chemistry, 2024; doi: 10.1038/s41557-023-01418-4)
Quelle: Universität des Saarlandes















