Auch der Nobelpreis für Chemie steht 2024 im Zeichen der künstlichen Intelligenz: Eine Hälfte des Preises geht an die Entwickler des KI-Systems „AlphaFold“, Demis Hassabis und John Jumper von Google Deepmind. Mit „AlphaFold“ ist es erstmals möglich, die dreidimensionale Faltung von Proteinen allein aus ihrer Aminosäuresequenz zu ermitteln – dies galt als „heiliger Gral“ der Proteinchemie. Die andere Hälfte des Nobelpreises geht an David Baker für die computergestützte Erzeugung künstlicher, in der Natur nicht vorkommender Proteine.
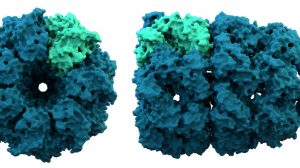
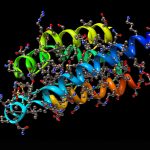
Proteine sind die Motoren des Lebens: Erst durch sie können unsere Zellen arbeiten, wachsen und verschiedenste Funktionen übernehmen. Auch Enzyme, Hormone und viele Immunbotenstoffe sind Proteine – ohne sie wäre kein Leben möglich. Doch damit ein Protein seine Funktion erfüllen kann, muss es nicht nur aus der korrekten Abfolge von Aminosäuren bestehen, auch seine dreidimensionale Form muss stimmen. Denn erst die Proteinfaltung bestimmt, ob ein Protein zum Enzym oder Zellbaustein wird, zum Antikörper oder zum Gerüst einer Hautschuppe.
Doch diese Faltung hat es in sich: Ein aus 100 Aminosäuren bestehendes Protein kann auf unzählige verschiedene Arten gefaltet sein – theoretisch existieren dafür 1047 mögliche Konfigurationen. Das macht es schwierig bis unmöglich, die 3D-Struktur eines Proteins allein anhand seiner chemischen Zusammensetzung vorherzusagen. Selbst die Kartierung mit modernster Labortechnik kann Jahre dauern. Deshalb waren bis zum Jahr 2020 erst rund ein Prozent aller Proteine entschlüsselt.
Die Vorhersage der Proteinstruktur allein auf Basis der Aminosäuresequenz galt lange als „heiliger Gral“ der Proteinchemie – es gibt dafür sogar einen speziellen Wettbewerb.

Demis Hassabis und John Jumper: die Väter von „AlphaFold“
Genau an diesem Punkt setzt der Durchbruch an, für den nun Demis Hassabis und John Jumper vom Google-Forschungszentrum Deepmind eine Hälfte des diesjährigen Chemie-Nobelpreises erhalten: Sie haben die künstliche Intelligenz „AlphaFold“ entwickelt, die die dreidimensionale Faltung von Proteinen schneller und treffsicherer als jeder Mensch vorhersagen kann. Bereits im Jahr 2021 hatte AlphaFold die Struktur von 350.000 Proteinen im menschlichen Körper entschlüsselt, inzwischen kennen wir dank seines Nachfolgemodells AlphaFold2 die Faltung von fast allen rund 200 Millionen bekannten Proteinen.
Das KI-System „AlphaFold“ basiert auf einem neuronalen Netzwerk, das mithilfe von hunderttausenden bekannten Proteinstrukturen darauf trainiert wurde, Gesetzmäßigkeiten in der Proteinfaltung zu erkennen. Die KI erkennt beispielsweise, welche Aminosäuren in der Proteinkette miteinander wechselwirken und ob sie die Kette dadurch an dieser Stelle biegen oder verknoten. Durch ständiges Abgleichen und Abwägen solcher Wechselwirkungen ermittelt die künstliche Intelligenz schließlich die komplette 3D-Struktur des Proteins – innerhalb von Minuten statt wie zuvor Jahren.
„Damit erfüllt das System einen seit 50 Jahren gehegten Traum: Die Vorhersage von Proteinstrukturen allein aus ihrer Aminosäuresequenz“, sagt Heiner Linke vom Nobelpreiskomitee für Chemie. Google DeepMind hat zudem den Code für AlphaFold2 öffentlich zugänglich gemacht und es damit Forschern aus aller Welt ermöglicht, dieses Werkzeug einzusetzen.

David Baker: Proteine nach Maß
Der dritte Preisträger, David Baker von der University of Washington in Seattle, hat seinen Weg ebenfalls mit der Entschlüsselung der Proteinfaltung begonnen. 1998 nahm er mit der von ihm entwickelten Software „Rosetta“ am Entschlüsselungs-Wettbewerb teil. Doch dies gab ihm den Anstoß, den umgekehrten Weg zu gehen: Könnte man dieses Computerprogramm nicht auch nutzen, um maßgeschneiderte Proteine herzustellen?
Tatsächlich gelang dies: Baker und sein Team entwickelten ihr Rosetta-Programm so weiter, dass sie die gewünschte dreidimensionale Struktur eines Proteins vorgeben können – beispielsweise die Bindungstasche eines gesuchten Enzyms. Das Programm ermittelt dann die Aminosäuresequenz, die genau diese dreidimensionale Proteinstruktur hervorbringt.
Der Durchbruch kam im Jahr 2003 mit einem Top7 genannten Protein: Dieses war mit 93 Aminosäuren nicht nur größer als alle zuvor synthetisch erzeugten Proteine, es hatte auch kein Vorbild in der Natur – es war eine Neukreation. Inzwischen haben auch Baker und seine Kollegen die Fortschritte in der künstlichen Intelligenz genutzt und ihr Rosetta-Programm durch ein KI-System verbessert.
„Neue Ära der biochemischen Forschung“
„Die Errungenschaften von David Baker, Demis Hassabis und John Jumper auf dem Feld des computergestützten Proteindesigns und der Proteinstruktur-Entschlüsselung sind fundamental“, erklärt das Nobelpreiskomittee zum diesjährigen Chemie-Nobelpreis. „Ihre Arbeit hat eine neue Ära der biochemischen und biologischen Forschung eröffnet, in der wir nun Proteinstrukturen auf eine Weise entwerfen und vorhersagen können, wie es nie zuvor möglich war.“
Die Fähigkeit, maßgeschneiderte Proteine zu erstellen, kann beispielsweise dabei helfen, neue Arzneimittel und Impfstoffe zu entwickeln. Sie kann aber auch Prozesse in der chemischen Industrie umweltfreundlicher machen. Das schnelle Entschlüsseln der Proteinstruktur wiederum trägt dazu bei, die in unseren Zellen aktiven Biomoleküle besser zu verstehen, aber auch, durch Proteinfehler und Fehlfaltungen ausgelöste Krankheiten besser zu diagnostizieren und zu behandeln.
Quelle: Nobel Foundation