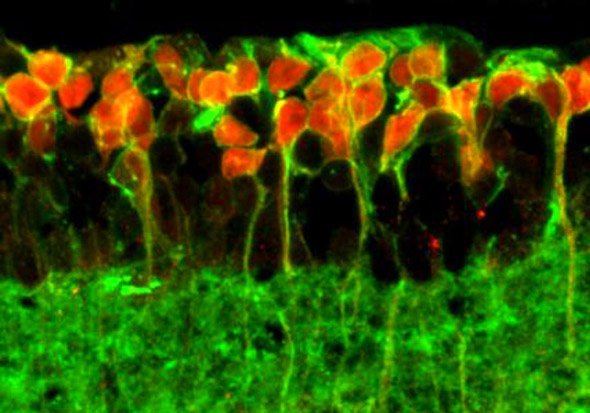
Von Blindheit geheilt: Forscher haben erblindeten Mäusen zu neuer Sicht verholfen. Dies gelang ihnen, indem sie die durch eine Erbkrankheit abgestorbenen Lichtrezeptoren im Auge durch eine neue „Lichtantenne“ ersetzten. Die Versuchstiere konnten damit wieder sehen. Dieser Ansatz könnte auch erblindeten Menschen das Augenlicht wieder zurückgeben, beispielswise Patienten mit Retinopathia pigmentosa oder einer Makuladegeneriation, schreiben die Forscher im Fachjournal „PLoS Biology“.
Bei der vererbten Augenkrankheit Retinopathia pigmentosa verlieren Betroffene nach und nach ihr Augenlicht. Die Lichtsensoren der Netzhaut, die sogenannten Fotorezeptoren, sterben ab. Oft kommt es bereits im Jugendalter zu ersten Symptomen wie Nachtblindheit. Im Laufe der Jahre werden die Augen immer weniger lichtempfindlich, bis die Patienten nach mehreren Jahrzehnten erblinden. Zwei bis drei Millionen Menschen sind weltweit von dieser bislang unheilbaren Erbkrankheit betroffen.
Neue Lichtantenne für die Zellen
Mit den Fotorezeptoren geht das erste Glied in der Kette der Signale zum Gehirn verloren, die Augen verlieren gewissermaßen die Antenne für das einfallende Licht. Der Rest der Kette ist jedoch noch vorhanden: „Auch wenn die Fotorezeptoren ihre Funktion verlieren, sind die darunter liegenden Nervenzellen, die normalerweise die visuelle Information erhalten und verarbeiten, noch voll funktionsfähig“, erläutert Sonja Kleinlogel von der Universität Bern.
Mit einem Ersatz für die defekten Rezeptoren könnten daher Patienten mit Retinopathia pigmentosa wieder sehen. Eine solche Therapie haben Kleinlogel und ihr Team nun an Mäusen getestet: „Wir haben eine neue ‚Lichtantenne‘ in die Zelle integriert, was dazu führte, dass praktisch der ganze Lichtreiz verarbeitet werden konnte“, erklärt Kleinlogel.
Lichtschalter ersetzt Andockstelle
Dazu haben die Wissenschaftler die sogenannten ON-Bipolarzellen der Netzhaut manipuliert. Diese Zellen erhalten normalerweise Signale von den Fotorezeptoren in Form des Botenstoffes Glutamat. Andockstelle für diese Signale ist der Glutamat-Rezeptor mGluR6. Die Zellen der Netzhaut verfügen jedoch auch über einen weiteren lichtempfindlichen Rezeptor, eine Art Lichtschalter, der für unseren Tag-Nacht-Rhythmus verantwortlich ist: das Melanopsin.
Aus diesen beiden Rezeptoren bauten die Forscher mit molekulargenetischen Methoden einen neuen Rezeptor zusammen: „Wir haben einfach die Glutamat-Andockstelle des mGluR6-Rezeptors durch die Lichtantenne von Melanopsin ersetzt“, führt Kleinlogel aus. Der Effekt dieses kombinierten Opto-mGluR6-Rezeptors: Die so therapierten Mäuse konnten wieder Tageslicht sehen und auf visuelle Reize reagieren.
Normaler Signalweg ohne Fremdkörper
Ein großer Vorteil der Methode ist, dass der normale Signalweg der Bipolarzellen erhalten bleibt. Außerdem sehen die Bipolarzellen den Opto-mGluR6-Rezeptor als „eigen“ und somit nicht als Fremdkörper an: „Da Melanopsin und mGluR6 beides natürlich vorkommende Proteine der Netzhaut sind, macht das eine Immunabwehr des Patienten äußerst unwahrscheinlich“, so Kleinlogel.
Eine auf diesem Ansatz basierende Therapiemethode könnte Menschen helfen, die durch den Verlust ihrer Fotorezeptoren erblindet sind. Auch bei altersbedingter Makuladegeneration könnte die Methode wirksam sein. Diese Augenkrankheit trifft etwa einen von zehn Menschen über 65 zu einem gewissen Grad. „Der Hauptvorteil von Opto-mGluR6 ist, dass Patienten wieder normales Tageslicht sehen könnten, ohne lichtintensivierende oder bildumwandelnde Brillen tragen zu müssen“, fügt Kleinlogel an.
Neue Rezeptoren nicht nur fürs Auge?
Darüber hinaus könnte die molekularbiologische Methode auch noch in vielen anderen Bereichen nützlich sein: Der mGluR6-Rezeptor gehört pharmakologisch bedeutenden Gruppe der GPCR-Rezeptoren. Diese sind auch im Gehirn weit verbreitet und sind ein Ziel vieler Medikamente.
Kleinlogel und ihr Team haben mit dem Opto-mGluR6-Rezeptor gezeigt, dass sich auf GPCR-Basis ein neuer Rezeptor herstellen lässt – dies eröffnet den Forschern zufolge auch neue Möglichkeiten, Krankheiten des Gehirns wie zum Beispiel Angststörungen, chronische Schmerzen, Depression oder Epilepsie zu behandeln. Bis dahin ist allerdings noch viel weitere Forschung nötig: „Es wird noch mindestens zwei bis drei Jahre in Anspruch nehmen, bis Opto-mGluR6 in der Klinik getestet werden kann.“ (PLoS Biology, 2015; doi: 10.1371/journal.pbio.1002143)
(Universität Bern, 08.05.2015 – AKR)