Wie ein Spiegelei in der Pfanne: Durchsichtige, gelöste Proteine können unter Stress oder Hitze verklumpen und trübe werden. Passiert dies in der Linse des Auges, droht dauerhafte Blindheit durch grauen Star. Münchner Wissenschaftler veröffentlichten in den Proceedings of the National Academy of Science nun, wie sie diese Krankheit in Zukunft zu verhindern hoffen.
Die Augenlinse des Menschen besteht aus einer hochkonzentrierten Proteinlösung, die ihr ihre hohe Brechkraft verleiht. Trotz dieses hohen Eiweißgehalts muss die Linse jedoch klar und lichtdurchlässig bleiben. Aus diesem Grund liegen hier einzigartige Bedingungen vor: Die Linsenzellen verzichten komplett auf die komplexe, in allen anderen Körperzellen vorhandene Maschinerie zum Auf- und Abbau von Proteinen. Stattdessen werden die Linsenproteine nur ein einziges Mal in der Embryonalentwicklung angelegt. Sie sind also so alt wie der Organismus selbst. Damit sie ein Menschenleben lang funktionieren, müssen die Eiweiße permanent in gelöstem Zustand gehalten werden. Verklumpen sie, führt das zu einer Trübung der Linse – grauer Star ist die Folge.
Alternative zur Operation
Bislang kann diese Erkrankung nur operativ, durch das Einsetzen einer künstlichen Linse, behandelt werden. Wäre jedoch der genaue Wirkmechanismus bekannt, der die Linsenproteine in ihrem gelösten Zustand erhält, könnte dies den Weg zu neuen Therapiemöglichkeiten eröffnen. Wie also schafft es die Zelle die Proteine so lange löslich zu halten? Verantwortlich hierfür sind zwei Schutzproteine, das sogenannte αA-Crystallin und sein Verwandter, das αB-Crystallin. Sie sind die bekanntesten Vertreter der Klasse der kleinen Hitzeschockproteine, die in vielen Körperzellen eine wesentliche Rolle spielen, denn sie bewahren andere Proteine davor, bei starker Hitze oder zellulärem Stress zu einem unbrauchbaren Knäuel zu verklumpen.
Wie diese Schutzproteine jedoch genau aussehen und wirken, war trotz intensiver Forschung lange unbekannt. „Die große Herausforderung bei der Analyse der beiden Crystalline liegt in ihrer großen strukturellen Vielfalt“, erklärt Johannes Buchner, Professor für Biotechnologie der Technischen Universität München. „Es liegt ein Gemisch ganz verschiedener Formen vor, die sich aus unterschiedlich vielen Untereinheiten zusammensetzen. Dies macht es sehr schwer, die einzelnen Strukturen voneinander zu unterscheiden.“
Puzzlespiel mit Schattenbildern
Zunächst gelang es den Wissenschaftlern, ein erstes Puzzleteil des großen Rätsels um das αB-Crystallin aufzudecken. Sie konnten mit dem Elektronenmikroskop die Molekularstruktur der wichtigsten Form des vielfältigen Proteins entschlüsseln. Die Information der zweidimensionalen elektronenmikroskopischen Bilder zu den vielfältigen dreidimensionalen Strukturen des αB-Crystallins wieder zusammen zu setzen gestaltete sich hierbei besonders schwierig.
„Stellen Sie sich vor, Sie haben lediglich mehrere Bilder des Schattens einer Kaffeetasse zur Verfügung und möchten daraus auf die Tasse selbst schließen“, veranschaulicht Sevil Weinkauf, Professorin für Elektronenmikroskopie am Department Chemie, den Sachverhalt. „Stellen Sie sich nun vor, Sie hätten nicht nur einen Tassentyp sondern ein ganzes Service an Tassen, die Sie aus ihren Schattenbildern zusammensetzen müssen. Genau diese anspruchsvolle Aufgabe konnten wir beim αB-Crystallin lösen.“
Molekularer Schalter
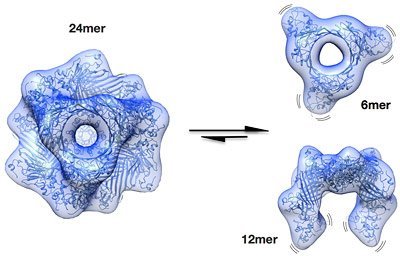
Heraus kam dabei ein Proteinkomplex mit 24 identischen Untereinheiten. Dieser Komplex kommt unter normalen Bedingungen, das heißt wenn die Zelle keinem Stress ausgesetzt ist, am häufigsten vor. Er stellt jedoch eine Ruheform dar und verhindert das Verklumpen der anderen Proteine nur wenig – es musste also noch einen molekularen Schalter geben, der das Schutzprotein in Gang setzt.
Genau diesen Aktivierungsmechanismus konnten die Wissenschaftler um Buchner und Weinkauf nun entschlüsseln: Gerät die Zelle unter Stress, beispielsweise durch Einwirkung von Hitze, werden Phosphatgruppen an eine bestimmten Region des Proteins angeheftet. Die negativen Ladungen dieser Phosphate lösen dann die Verknüpfungen zwischen den Untereinheiten – der große Komplex zerfällt in kleinere, die nur noch aus sechs oder zwölf Untereinheiten bestehen. Durch diesen Zerfall werden die Regionen am einen Ende der neuen kleinen Komplexe flexibler und ermöglichen es dem Molekül, nun an verschiedene Partner anzudocken und diese vor dem Verklumpen zu bewahren – das Schutzprotein ist aktiv.
Neue Therapiemöglichkeiten gegen grauen Star und Krebs
Die neu gewonnenen Erkenntnisse zum Wirkmechanismus des αB-Crystallins bilden die Grundlage zu neuen Therapiemöglichkeiten. Zur Behandlung des grauen Stars wäre beispielsweise ein Medikament denkbar, das – eingespritzt in die Augenlinse – den Aktivierungsmechanismus des αB-Crystallins in Gang setzt und so die getrübte Linse wieder transparent werden lässt. Doch auch in anderen Gewebezellen spielt das αB-Crystallin eine Rolle. In Krebszellen etwa ist das Protein zu aktiv und hindert die Zellen am programmierten Zelltod – hier würden neue Medikamente eher auf eine Hemmung des Proteins abzielen.
(PNAS, 2013; doi: 10.1073/pnas.1308898110)
(Technische Universität München, 24.10.2013 – AKR)