Bei der Fischer-Tropsch-Synthese wird aus den Vorprodukten CO2 und Wasserstoff in einem mehrschrittigen Verfahren E-Fuels wie Rohbenzin, E-Kerosin oder E-Diesel produziert. Diese bestehen aus einem Gemisch verschiedener ketten- und ringförmiger Kohlenwasserstoffe. Um diese Verbindungen aus CO2 herzustellen, müssen die Gasmoleküle über Kohlenstoff-Kohlenstoffbindungen miteinander verknüpft werden.
Fischer-Tropsch-Synthese
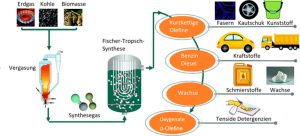
Für die Fischer-Tropsch-Synthese von E-Fuels benötigt man zuerst das Vorprodukt Kohlenstoffmonoxid. Um das Gas herzustellen, lässt man Wasserstoff und CO2 bei hohen Temperaturen und hohem Druck reagieren. Es entsteht ein Gasgemisch aus Wasser(dampf) und Kohlenstoffmonoxid – sogenanntes Syngas. Dann führt man das Kohlenmonoxid in einem Reaktor abermals mit Wasserstoff zusammen.
Dort spalten Cobalt- oder Eisen-Katalysatoren die Gase auf – so können neue Kohlenstoff-Kohlenstoff-Bindungen entstehen. Eine komplexe Abfolge von Reaktionen führt dabei zur schrittweisen Verlängerung der Kohlenwasserstoffketten. Die zugrundeliegenden Reaktionen sind zwar schon seit knapp 100 Jahren bekannt, dennoch haben Chemiker erst kürzlich neue Details aufgedeckt, mit deren Hilfe die Ausbeute noch weiter erhöht werden könnte.
Vom synthetischen Rohöl zum E-Fuel
Je nach Wahl der Katalysatoren, der Reaktionsbedingungen und des Verhältnisses der Anfangsgase entsteht bei der Fischer-Tropsch-Synthese ein Gemisch aus einfachen Kohlenwasserstoffketten verschiedener Länge (Alkane), Ketten mit Doppelbindungen (Alkene), Alkohole, Aldehyden und weiteren Kohlenwasserstoffverbindungen. Sie ähneln darin dem fossilen Erdöl.














