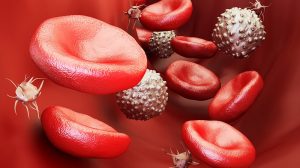
Eine ganze Reihe von Versuchen zu künstlichem Blut basieren auf dem Blutfarbstoff Hämoglobin – trotz seiner toxischen Effekte. Um das Sauerstofftransport-Molekül sicher außerhalb der roten Blutkörperchen einsetzen zu können, verfolgen Wissenschaftler zwei Strategien: das Hämoglobin zu polymerisieren oder es in einer künstlichen Hülle zu verpacken.

Variante 1: Weniger giftig durch Vernetzung
Die erste Sorte von hämoglobinbasierten Blutersatz-Präparaten beruht auf einer chemischen Vernetzung der Hämoglobin-Moleküle. Durch diese Polymerisation entstehen Makromoleküle, die zwar noch immer weit kleiner und instabiler sind als ein rotes Blutkörperchen. Die Vernetzung senkt aber die toxische Wirkung des puren Hämoglobins, weil die Moleküle nicht mehr so unkontrolliert in Gewebe und Organe eindringen können. Das verringert die Nebenwirkungen – so die Hoffnung.
Allerdings haben sich Kunstblut-Kandidaten nach diesem Ansatz bislang als nur bedingt erfolgreich erwiesen. Das vom Northfield Forschungslabor im Chicago entwickelte Präparat „PolyHeme“ wurde Anfang der 2000er Jahre in einer klinischen Studie der Phase 3 getestet. Weil aber zu viele Patienten erhöhten Blutdruck, Entzündungen und Organschäden bekamen, lehnte die US-Arzneimittelbehörde FDA eine Zulassung im Jahr 2009 ab.
Zwei Kandidaten mit bedingtem Erfolg
Das einzige bislang zur Behandlung von Menschen zugelassene Hämoglobin-Kunstblut besteht aus polymerisiertem Rinder-Blutfarbstoff. Seit 2001 darf Hemopure in Südafrika bei Operationen eingesetzt werden, wenn kein Spenderblut zur Verfügung steht oder eine Bluttransfusion aus anderen Gründen nicht möglich ist. Hauptgrund für die Zulassung war allerdings die pure Not: Im südlichen Afrika sind Blutkonserven und Blutspenden wegen der vielen HIV-Fälle oft mit Aids-Viren verseucht und daher unbrauchbar. In anderen Ländern ist dieses Kunstblut aber nicht zugelassen.