Egal ob als Impfstoff oder RNA-Medikament: Wenn man messenger-RNA als Wirkstoff in eine Zelle bringen möchte, muss man drei große Probleme überwinden: ihre Instabilität, ihre entzündungsfördernde Wirkung und die geringe Passierbarkeit der Zellmembran für das RNA-Molekül. Lange galten diese Hürden als nahezu unüberwindbar, weshalb die RNA-Technologie trotz ihres theoretisch enormen Potenzials für die Medizin nur am Rande erforscht wurde.

Schutz vor verfrühtem Abbau
Inzwischen jedoch hat sich die Lage geändert. Dank der hartnäckigen, von vielen Rückschläge geprägten Arbeit von hunderten Wissenschaftlern weltweit ist es der Forschung gelungen, für alle drei Probleme Lösungen zu entwickeln. Das erste ist die Instabilität: Weil die mRNA nur als Bote dient und entbehrlich wird, sobald ihr Code in den zellulären Proteinfabriken ausgelesen wurde, beseitigt die Zelle „nackte“ mRNA relativ schnell. Spezielle Enzyme, sogenannte RNasen, lagern sich am Strangende der mRNA an und bauen sie ab.
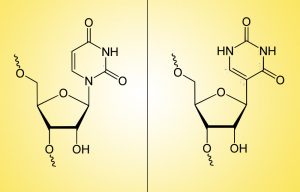
Inzwischen weiß man, dass sich dieser Abbau durch einige gezielte Modifikationen an den nicht zum Proteincode gehörenden Enden der RNA-Stränge umgehen oder zumindest hinauszögern lässt. Heutige RNA-Wirkstoffe, darunter auch die mRNA-Impfstoffe von BioNTech/Pfitzer und Moderna, haben daher spezielle Endkappen am 5′-Ende und veränderte Basenabfolgen am gegenüberliegenden Endstück, dem Poly-Tail-A. Auch der auf diesen „Schwanz“ folgende 3-UTR-Abschnitt, ein ebenfalls nicht für die Proteinproduktion ausgelesener Teil der Boten-RNA, ist modifiziert.
Lipid-Nanopartikel als Stabilisator und Einschleuse-Hilfe
Ein zweiter „Trick“ hilft sowohl gegen das Problem der Instabilität wie auch bei der Aufnahme der RNA in die Zelle : die Verpackung. In den mRNA-Impfstoffen gegen Corona und den meisten im Test befindlichen RNA-Wirkstoffen wird der Ribonukleinsäure-Strang in einem Lipid-Nanopartikel eingeschlossen. Dieses winzige Fettbläschen besteht aus einer Mischung aus vier verschiedenen Lipiden. Zwei dieser Fette, darunter ein Cholesterin und ein weiteres ungeladenes Lipid stabilisieren die Struktur des Nanopartikels, ein weiteres, meist ein Polyethylenglykol (PEG), sorgt für gute Aufnahme und Verträglichkeit.