Schon in der Schule lernen wir, dass Edelgase „bindungsscheu“ sind: Helium, Neon, Xenon und Co gehen kaum chemische Bindungen mit anderen Elementen ein – jedenfalls nicht freiwillig. Denn diese Gase besitzen bereits die energetische günstige Elektronenkonfiguration, die alle anderen Elemente anstreben: Ihre äußeren Elektronenschalen sind komplett gefüllt.

Helium unter Druck
Besonders „unsozial“ ist das leichteste Edelgas Helium: Unter normalen Bedingungen existiert keine einzige stabile Verbindung dieses Elements. Kein Wunder: „Sein Ionisationspotenzial ist das höchste von allen Elementen und seine Elektronenaffinität ist gleich Null“, erklärt Atem Oganov vom Moskauer Institut für Physik und Technologie. Zwar lässt sich das Edelgas unter hohem Druck auf Reaktionen ein, die resultierenden Moleküle sind jedoch nicht stabil und zerfallen schnell wieder.
Doch Oganov und seinem Team ist es gelungen, das bindungsscheue Element doch in eine stabile Paarung zu zwingen. In ihrem Experiment hatten die Forscher ein Gemisch von Natrium und Helium in einer Diamantstempel-Presse enormen Drücken ausgesetzt. Mittels Röntgenkristallografie und Raman-Spektroskopie beobachteten sie dabei den Zustand der Mischung. Sie stellten fest: Ab einem Druck von 113 Gigapascal bahnt sich ein Wandel an. Aus dem Gemisch der beiden Elemente wird unter Energieabgabe eine kristalline Verbindung.
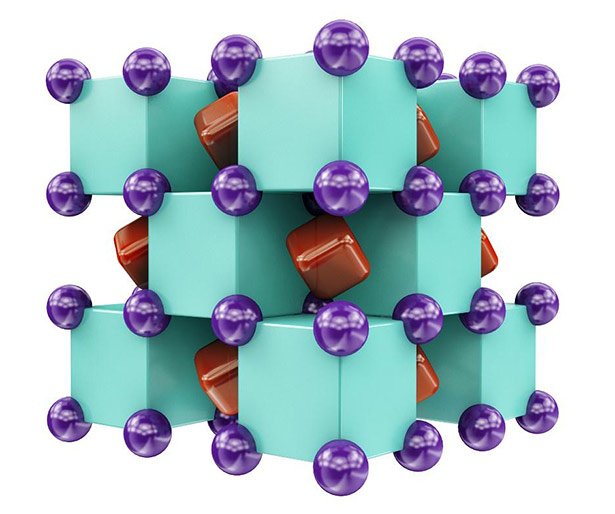
Ungewöhnlicher Kristall
„Die Verbindung, die wir entdeckt haben, ist allerdings ziemlich ungewöhnlich“, sagt Oganov. Auf den ersten Blick ähnelt das Na2He einem ionischen, salzähnlichen Kristall. In diesem bilden die Heliumatome ein kubisches Gitter – ähnlich einem 3D-Schachbrett, bei dem jedes schwarze Feld von Helium besetzt ist. Die Räume dazwischen sind jedoch abwechselnd von Natrium und von einem Elektronenpaar belegt.