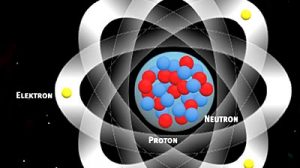
Supraleitende Materialien bestehen wie die meisten Festkörper aus Kristallen. Darin organisieren sich ihre Atome zu einem regelmäßigen räumlichen Gitter. Die Natur liebt Ordnung, falls diese hilft, Energie zu sparen. Und das gelingt den Atomen in Kristallen, weil sie sich bestimmte Elektronen untereinander teilen können. Diese Elektronen sorgen für den Kitt, die chemische Bindung, zwischen den Atomen. Das funktioniert nur dank der Quantenphysik: Weil Elektronen als Quantenteilchen auch räumlich ausgedehnte Wellen sind, können sie benachbarte Atome miteinander verbinden.
Elektronen mehr als nur Kristallkitt
In Metallen und Halbleitern wirken allerdings nicht alle Elektronen allein als Kristallkitt. Ein Teil von ihnen entwischt den Atomen und bewegt sich nahezu frei durch das Gitter, wobei sie dafür in Halbleitern eine gewisse Energiezufuhr benötigen. Diese freien Leitungselektronen tragen den elektrischen Strom. Die „Atomrümpfe“ behalten durch den Verlust eine positive elektrische Ladung zurück.
„Durch einen perfekten Kristall könnten die Leitungselektronen sich sogar ohne Widerstand bewegen“, erklärt Frank Steglich vom Max-Planck-Institut für Chemische Physik fester Stoffe in Dresden. Dafür sorgt die gleichmäßige Anordnung der Atome: Passen die Abstände der Berge und Täler der Elektronenwelle zu den Distanzen zwischen den Atomen, kann das Elektron ungehindert durch den Kristall hüpfen.
Perfekte Kristalle existieren nicht
Doch perfekte Kristalle gibt es nicht. Jedes Kristallgitter weist Webfehler auf. Sie passen nicht zum Takt der Elektronenwellen, weshalb diese an ihnen regelrecht abprallen. Und selbst wenn es Kristalle mit perfekt geordneten Atomen gäbe, würde die Temperatur den widerstandslosen Stromfluss vereiteln. Denn je höher sie steigt, desto stärker und schneller schwingt das Atomgitter des Kristalls – wie eine Matratze, auf der man wild hüpft. Auch das stört die kristalline Perfektion und behindert die Wellen der Leitungselektronen.