
Korrosion ist ein Problem von großer wirtschaftlicher Bedeutung. Werden die Kosten für Korrosion und Korrosionsschutz in den westlichen Ländern doch auf etwa vier Prozent des Bruttosozialprodukts geschätzt. Das sind rund 80 Milliarden Euro pro Jahr allein in Deutschland.
Barriere zwischen Bauteil und aggressiven Umwelteinflüssen
Bei metallischen Werkstoffen sind organische Korrosionsschutzschichten, zum Beispiel auf Epoxy- oder Polyurethanbasis, heute die Schutzmaßnahme der Wahl. Eine solche Schicht bildet eine Barriere zwischen korrosionsgefährdetem Bauteil und aggressiven Umwelteinflüssen. Doch wird die Schicht beschädigt, kommt es in den Defekten schnell wieder zu Korrosion. Mit verschiedenen Strategien versuchen Materialforscher das zu verhindern: So sollen in den Beschichtungen aktive Korrosionsschutzpigmente Wirkstoffe, sogenannte Inhibitoren, freisetzen und die Korrosion stoppen.
Zinkbeschichtungen schützen Stahl
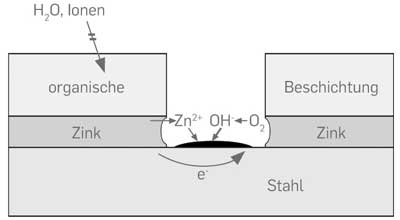
Zum Schutz von Stahl setzt man zusätzlich Zinkbeschichtungen ein, die als erste Schicht auf dem Stahl aufgetragen werden. Zink ist dabei das unedlere Metall und fungiert als Anode in einer so genannten galvanischen Kopplung zwischen Zink und Stahl (Kathode): Wenn die verletzte Zinkschicht korrodiert, setzt Zink Elektronen frei, die vom Stahl (Eisen) aufgenommen werden. Damit wird Stahl auf das niedrigere Potenzial von Zink gezogen (polarisiert).
Dieser elektrochemische Prozess bewirkt einen so genannten kathodischen Korrosionsschutz. Auf dem Stahl findet bei den niedrigen Potenzialen nur die kathodische Reduktion von Sauerstoff aus der Luft statt, wodurch Stahl geschützt bleibt. Die dabei entstehenden Hydroxyl-Ionen verschieben den pH-Wert auf dem Stahl ins Alkalische, was die Korrosionsgefahr für den Stahl zusätzlich verringert.


















