Vancomycin galt lange Zeit als „Mittel der letzen Wahl“ gegen schwere Krankenhausinfektionen. Denn das Antibiotikum wirkt auch gegen Keime, die Beta-Lactamasen produzieren und damit bereits resistent gegen Penicilline sind. Sein Schutz vor diesen bakteriellen Abwehrtricks beruht darauf, dass Vancomycin nicht am Bindeprotein der Bakterien ansetzt, sondern direkt an freien Aminosäure-Enden im Molekülnetz der Zellwand. Durch seine Anlagerung verhindert es eine Quervernetzung und erzeugt Löcher, die letztlich zum Platzen der Bakterienzellen führen.
Enterokokken werden resistent
Aber 1987 wurde auch diese Waffe stumpf: Ärzte entdeckten die ersten Vancomycin-resistenten Enterokokken (VRE). Diese gramnegativen Bakterien hatten in ihrer Zellwand eine Aminosäure durch einen Zucker ersetzt und verhinderten so effektiv das Andocken des Antibiotikums. Inzwischen gelten mehr als 90 Prozent aller in amerikanischen Intensivstationen isolierten Stämme von Enterococcus faecium als mindestens zweifach resistent: Die normalerweise gegen Sepsis und Herzbeutelentzündungen verabreichte Kombination aus Vancomycin und dem Penicillin Ampicillin wirkt bei ihnen nicht mehr.
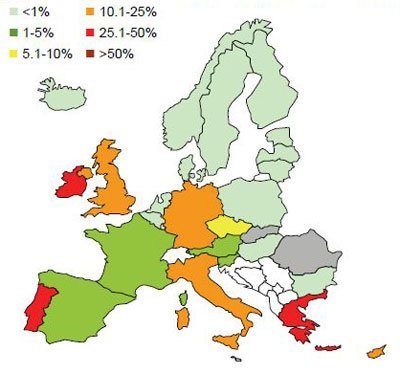
Doch es sollte noch schlimmer kommen. Denn auch wenn Vancomycin gegen gramnegative Erreger wie Enterokokken oder Escherichia coli zunehmend wirkungslos wurde, war es noch immer die beste Waffe gegen den multiresistenten Krankenhauskeim Staphyolococcus aureus. Das grampositive Bakterium gehört zu den ersten Krankheitserregern, die das Abwehrenzym Beta-Lactamase gegen Penicillin entwickelten und damit gegen diese Wirkstoffgruppe unempfindlich wurden. Nach ihrer fehlenden Reaktion auf das Testantibiotikum Methicillin auch als methicillin-resistenter Staphylococcus aureus (MRSA) bezeichnet, haben sie sich seither extrem ausgebreitet. Heute sind bereits 70 bis 80 Prozent aller in Proben nachgewiesenen MRSA-Stämme immun gegen zahlreiche Beta-Lactam-Antibiotika.
50.000 MRSA-Opfer jährlich allein in Europa
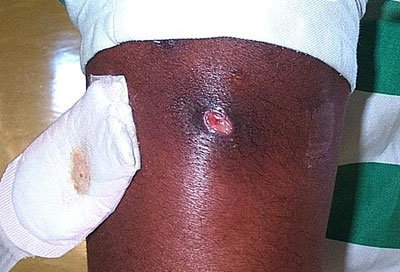
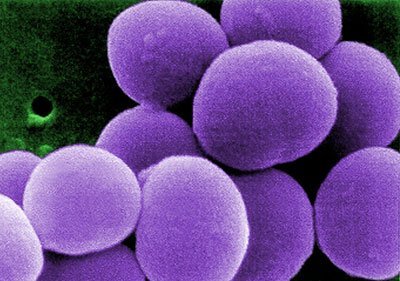
Für Gesunde meist unschädlich, besiedeln die kugelförmigen Mikroben Haut und Schleimhäute von bis zu 30 Prozent aller Menschen. Bei immungeschwächten Patienten jedoch können die durch eine Kapsel vor Fresszellen des Immunsystems geschützten Bakterien schwere Hautinfektionen, Lungen- und Herzentzündungen sowie das Toxic-Shock-Syndrom auslösen. Breitet sich der Erreger in großer Menge über das Blut in Organen und Geweben aus, ist seine Bekämpfung schwierig, die resultierende Sepsis endet häufig tödlich.