Jenaer Wissenschaftler sind bei der Erforschung der Alzheimer-Erkrankung einen entscheidenden Schritt weitergekommen. Ihnen ist es mithilfe der Proteinkristallographie gelungen, die atomare Struktur des Amyloid-Vorläuferproteins (APP) zu enthüllen. Spaltprodukte dieses Eiweißes können Alzheimer auslösen, APP erfüllt aber auch wichtige biologische Funktionen.
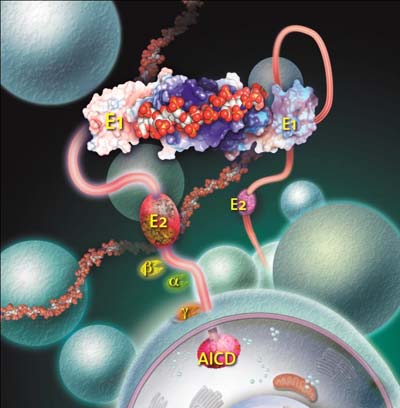
Alzheimer ist die häufigste Form der Altersdemenz. Ausgelöst wird diese Krankheit durch unlösliche Eiweißbestandteile, die sich in der Umgebung von Nervenzellen ablagern und dort Plaques bilden. Diese Proteinklumpen – auch Beta-Amyloide genannt – schädigen die Nervenzellen, bis diese schließlich absterben. Mittlerweile ist bekannt, dass die neurotoxischen Eiweißablagerungen aus Spaltprodukten eines bestimmten Makromoleküls bestehen, das auf der Membran von Nervenzellen zu finden ist. Amyloid-Vorläufer-Protein (APP) wird dieses Membranmolekül genannt.
Plaquebildung unerwünschter Nebeneffekt
„Es ist unwahrscheinlich, dass der biologische Sinn dieses Membranmoleküls darin besteht, Plaques zu bilden, Nervenzellen zu töten und damit eine der schlimmsten Formen von Demenz auszulösen. Man vermutet, dass dies eher ein unerwünschter Nebeneffekt ist“, sagt Dr. Manuel Than vom Leibniz-Institut für Altersforschung, Fritz-Lipmann-Institut in Jena. Der Forscher analysiert mit seinem Team die atomare Struktur des Amyloid-Vorläufer-Proteins, um dessen biologische Grundfunktionen ergründen zu können.
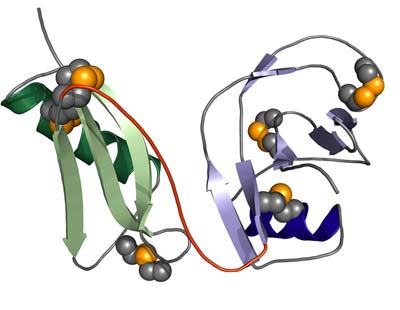
Den Jenaer Forschern ist es nun gelungen, einen wesentlichen Teil dieses Proteins – die so genannte E1-Domäne – zu kristallisieren und dessen atomare Struktur aufzuklären. Durch Bestrahlung von Proteinkristallen mit Röntgenstrahlung erzeugten die Wissenschaftler so genannte Beugungsdaten. Durch ein computergestütztes Verfahren wurden diese dann in ein hochaufgelöstes, dreidimensionales Abbild oder „Modell“ des Moleküls umgewandelt. Dieses Modell beschreibt den atomaren Aufbau und die räumliche Struktur des Moleküls. Dabei zeigte sich, dass die E1-Domäne eine starre Faltungseinheit bildet. „Anders als bisher angenommen, stellen die bisher bekannten Funktionsabschnitte, eine Kupferbindungsstelle und ein Wachstumsfaktor-ähnlicher Abschnitt, eine funktionale Einheit dar“, sagt Than.