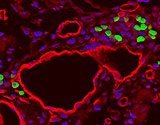
Adulte Stammzellen spielen nach unserer Geburt möglicherweise eine wesentlich geringere Rolle beim Wachstum von Blutgefäßen als bisher angenommen. Das ist das Ergebnis einer neuen Studie von Wissenschaftlern am Max-Planck-Institut für physiologische und klinische Forschung in Bad Nauheim.
Die Forscher aus der Arbeitsgruppe von Prof. Wolfgang Schaper hatten bei speziellen Mauslinien untersucht, ob Knochenmarks-Stammzellen bei der Arteriogenese, einer Form des Wachstums von Arterien aus bereits vorhandenen kleinsten Blutgefäßen, tatsächlich in die Gefäßwand eingebaut werden. Dieser Wachstumsprozess setzt beispielsweise beim chronischen Verschluss einer Herzkranz-Arterie ein und kann zur Bildung eines natürlichen Gefäß-Bypasses führen, der im Idealfall Defizite in der Blutversorgung kompensieren kann. Doch entgegen den Befunden anderer Forschergruppen zeigen die Max-Planck-Wissenschaftler, dass die Stammzellen offenbar unfähig sind, während der Arteriogenese die Funktion von Zellen der Gefäßwand zu übernehmen. Die Ergebnisse ihrer Studie wurden jetzt in der internationalen Fachzeitschrift „Circulation Research“ der American Heart Association veröffentlicht.
Zweifel an Differenzierungsfähigkeit
Es ist noch gar nicht lange her, dass gängige Vorstellungen, wonach die Entstehung neuer Blutgefäße aus primitiven Stammzellen auf den embryonalen Lebensabschnitt beschränkt sei, in Frage gestellt wurden. Vielmehr schlug man vor, aus dem Knochenmark kommende adulte Stammzellen würden auch noch nach der Geburt im Körper zirkulieren und in sich neu entwickelnde Blutgefäße eingebaut. Mehr noch, die Transplantation dieser Stammzellen schien bei Krankheiten wie Herzinfarkt oder Schlaganfall eine rasche Erneuerung der betroffenen Blutgefäße zu versprechen. Doch inzwischen wurden bereits in einigen Studien erste Zweifel daran laut, ob sich Knochenmarkstammzellen unter diesen Umständen tatsächlich in Organ-spezifische Zellen differenzieren könnten.
Vor diesem Hintergrund haben sich Wissenschaftler des Max-Planck-Instituts für physiologische und klinische Forschung intensiv mit der Frage beschäftigt, welche Rolle die Knochenmarkstammzellen speziell beim adaptiven Wachstum von Blutgefäßen spielen. Diese Remodellierung des arteriellen Systems, nachdem sich eine wichtige Arterie – zum Beispiel durch Arteriosklerose oder Thrombose – verschlossen hat, bezeichnet man als Arteriogenese.