Eine Kombination aus zwei einfachen Chemikalien könnte künftig helfen, Wasserstoff reversibel zu speichern und gleichzeitig Kohlendioxid aufzunehmen. Ein solcher chemischer Wasserstoffspeicher ermöglicht den sicheren Transport und die Lagerung des Energiegases – eine für die Energiewende entscheidende Voraussetzung. Möglich wird die neue Wasserstoff-„Batterie“ durch einen chemischen Kreislauf, bei dem ein Mangankatalysator, Ameisensäure und die Aminosäure Lysin eine Schlüsselrolle spielen.
Wasserstoff gilt als wichtiger Energieträger der Zukunft. Er kann mithilfe von Strom aus Wind und Sonne durch Elektrolyse von Wasser gewonnen werden und gibt bei seiner Verbrennung kein CO2 ab. In Brennstoffzellen kann Wasserstoff zudem als elektrochemischer Antrieb dienen. Der Haken jedoch: Wasserstoff lässt sich wegen seiner geringen Dichte und der Explosionsgefahr in Gasform nicht gut transportieren. Für mobile Anwendungen muss er daher verflüssigt oder chemisch gebunden werden.
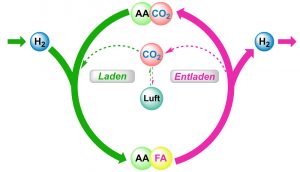
Ein reversibler chemischer Wasserstoffspeicher
An genau diesem Punkt setzt der neue Wasserstoffspeicher von Duo Wei vom Leibniz-Institut für Katalyse in Rostock und seinen Kollegen an. Sie haben ein katalytisches System entwickelt, das Wasserstoff chemisch speichert und in hochreiner Form und mit hoher Ausbeute wieder abgeben kann. Das System folgt damit dem Prinzip einer elektrischen Batterie, nur dass die Wasserstoff-Batterie statt mit elektrischem Strom mit Wasserstoff geladen und entladen wird.
Zwar gibt es bereits einige Konzepte für solche chemischen Wasserstoffspeicher. „Die meisten von ihnen benötigen aber kostspielige, auf Edelmetallen wie Ruthenium, Rubidium oder Iridium basierende Katalysatoren“, erklärt das Forschungsteam. Hinzu kommt, dass die Reaktionen zur Speicherung und Freisetzung des Wasserstoffs jeweils unterschiedliche Bedingungen brauchen, was einer effektiven „Akku“-Funktion entgegensteht.
Kombi aus Ameisensäure und Aminosäure als Kernkomponenten
Im Gegensatz dazu haben Wei und seine Kollegen nun eine Wasserstoff-Batterie entwickelt, die mit einem vergleichsweise günstigen Mangankomplex als Katalysator funktioniert und unter einheitlichen Bedingungen Wasserstoff aufnehmen und abgeben kann – in einem echten Kreislauf. Zentrales Element dieses Kreislaufs ist neben dem Mangan-Katalysator das einfache organische Molekül Ameisensäure (HCOOH), das als Speichermedium für den Wasserstoff dient.
Die Ameisensäure entsteht, wenn die zweite Kernkomponente, die Aminosäure Lysin unter Einfluss des Mangan-Katalysators mit Kohlendioxid aus der Luft und dem zugeführten Wasserstoff zur Ameisensäure reagiert. Alternativ ist auch die Reaktion zur einem Formiat, dem Salz der Ameisensäure möglich. Der Wasserstoff ist nun chemisch gebunden. Für die Wiederfreisetzung wird das Formiat in Gegenwart der beiden Reaktionshelfer Lysin und Mangan-Komplex wieder dehydrogeniert, es entstehen CO2 und Wasserstoff.
Lysinat bindet CO2 und schließt den Kreislauf
In ersten Tests dieses Kreislaufs erzielten die Forschenden bereits eine Ausbeute von mehr als 80 Prozent, bei zehn Zyklen hintereinander lag sie immerhin noch bei gut 72 Prozent. Das Problem jedoch: „Das Ziel einer praktisch nutzbaren, wiederaufladbaren Wasserstoff-Batterie wird so nicht erreicht“, schreiben Wei und seine Kollegen. Weil das CO2 bei jeder Dehydrogenierung frei wird, muss es nachgefüllt werden und ein geschlossener Kreislauf, bei dem nur Wasserstoff rein- und rausgeht, ist nicht möglich.
Deshalb optimierten die Chemiker ihr System, indem sie statt Lysin das Kaliumsalz dieser Aminosäure verwendeten. Tests ergaben, dass das Kaliumlysinat 99,9 Prozent des bei den Reaktionen freiwerdenden CO2 aufnehmen kann und damit den CO2-Kreislauf schließt. „Wir halten das CO2 dauerhaft in unserem Reaktionssystem fest“, erklärt Weis Kollege Matthias Beller. Die Wasserstoff-Batterie muss nur noch einmal zu Beginn mit Luft befüllt werden, der Rest läuft dann im Kreislauf ab.
Hohe Effizienz
Durch diese Optimierung erhöhte sich auch die Ausbeute des wiedergewinnbaren Wasserstoffs: Das System kann Wasserstoff mit 93-prozentiger Effizienz als Formiat binden und gibt es zu 99 Prozent wieder ab. Über zehn Zyklen gerechnet liegt die Effizienz für Wasserstoffspeicherung und -freisetzung bei insgesamt mehr als 80 Prozent, wie das Team berichtet. Das beim Entladen dieser Wasserstoff-Batterie wiedergewonnen Wasserstoffgas sei zudem von hoher Reinheit.
„Diese Methode repräsentiert damit der produktivsten Kombinationen von CO2-Bindung und Formiat-Dehydrogenierung auf Basis eines nicht aus Edelmetallen bestehenden Katalysators“, schreiben Wei und seine Kollegen. Das System ebne den Weg zum Aufbau einer CO2-neutralen chemischen Wasserstoffspeicherung auf Basis ungiftiger Komponenten. Das Team hat für ihre Wasserstoff-Batterie bereits ein Patent beantragt. (Nature Energy, 2022; doi: 10.1038/s41560-022-01019-4)
Quelle: Leibniz-Institut für Katalyse














