Good Vibrations: Ein verblüffend simples Hilfsmittel könnte die Wasserstoff-Gewinnung effizienter machen. Denn wenn man die Elektrolyse hochfrequenten Schallwellen aussetzt, steigern die Vibrationen die Wasserstoffausbeute um das 14-Fache, wie ein Experiment nun belegt. Der Grund: Zum einen verhindert die akustische Beschallung die Ansammlung störender Gasblasen an den Elektroden. Zum anderen werden H2O-Moleküle aus ihrem Verbund herausgeschüttelt, was die Wasserspaltung erleichtert.
„Grüner“ Wasserstoff gilt als wichtiger Baustein der Energiewende und als klimafreundlicher Energieträger. Für seine Gewinnung werden Wassermoleküle in Elektrolyse-Anlagen in Sauerstoff und Wasserstoff zerlegt. Die dafür nötige Energie kann Sonnen- und Windstrom liefern oder auch das Sonnenlicht direkt. Um die Effizienz dieser Elektrolyseure zu erhöhen, bestehen ihre Elektroden meist aus teuren Platinmetallen, außerdem wird eine stark saure oder alkalische Elektrolytlösung verwendet – was zu schneller Korrosion der Anlagen führt.
CC-by-nc-nd 4.0
Elektrochemie mit Vibrationen
Doch es geht auch anders, wie nun Yemima Ehrnst von der RMIT University in Melbourne und ihre Kollegen demonstrieren. Sie hatten für ihre Studie nach Möglichkeiten gesucht, um die Wasserspaltung auch mit neutralen Elektrolyten und weniger teuren Elektrodenmaterialien effizienter zu machen. Typischerweise ist die Wasserstoffausbeute bei solchen Systemen um mehrere Größenordnungen geringer, unter anderem, weil sich das entstehende Gas an den Elektroden sammelt und die weitere Reaktion behindert.
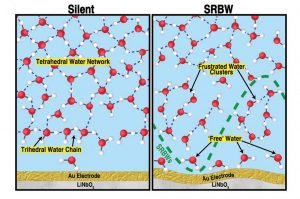
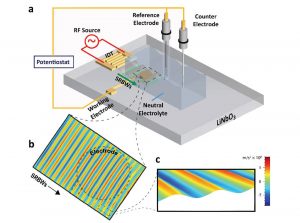
Um Abhilfe zu schaffen, testeten die Wissenschaftler was passiert, wenn man ein solches Elektrolysesystem mit hochfrequenten Schallwellen in Vibrationen versetzt. Dafür konstruierten sie eine elektrochemische Reaktionszelle, deren Basis das piezoelektrische Material Lithiumniobat (LiNbO3) bildete. Dieses lässt sich in elektromechanische Schwingungen im Megahertzbereich versetzen und erzeugt so hochfrequente Schall- und Oberflächenwellen im flüssigen Medium der elektrochemischen Zelle. Den neutralen Elektrolyt bildete Natriumphosphat.