Nächster Schritt zur Wasserstoff-Produktion auf hoher See: Forschende haben ein Elektrolysesystem entwickelt, das auch mit Meerwasser effizient funktioniert – ohne dass das Salzwasser zuvor entsalzt und vorbehandelt werden muss. Möglich wird dies durch einen speziell beschichteten Katalysator, der die Elektroden vor Korrosion und Ablagerungen schützt. Er fängt die bei der Elektrolyse gebildeten reaktiven Ionen ab, bevor sie Schaden anrichten können, wie die Wissenschaftler in „Nature Energy“ berichten.
Die Erzeugung von grünem Wasserstoff auf hoher See oder an der Meeresküste hätte gleich mehrere Vorteile: Klimafreundlichen Strom für die Elektrolyse können Offshore-Windanlagen liefern. Für diese dient der Wasserstoff wiederum als chemischer Energiespeicher, durch den Stromüberschüsse abgepuffert werden können. Außerdem ist der wichtigste Rohstoff für die Wasserstoffgewinnung am und im Meer reichlich vorhanden – sollte man meinen.
Korrosion und Ablagerungen
Aber ganz so einfach ist es leider nicht: Gängige Elektrolysesysteme vertragen kein Meerwasser. Die gelösten Salze im Meerwasser werden bei der Wasserspaltung frei und reagieren mit dem Material der Elektroden. Als Folge kommt es zu rapider Korrosion und zu blockierenden Ablagerungen, durch die die Elektrolyseure unbrauchbar werden. Deshalb muss Meerwasser bisher zuerst entsalzt werden, alternativ setzt man starke Säuren oder Basen ein, um die freiwerdenden Ionen zu binden.
Hinzu kommt: „Die Aktivität von Katalysatoren für die Sauerstoffproduktion an der Anode und die Wasserstoffgewinnung an der Kathode ist in neutralem Meerwasser sehr gering“, erklären Jiaxin Guo von der Tianjin Universität in China und seine Kollegen. „Deshalb wird eine sehr viel höhere Spannung benötigt. Das löst aber erst recht eine schädliche Korrosion und Oxidation durch Chlorid-Ionen aus.“
Kombi aus Chromoxid und Kobaltoxid als Katalysator
Als Lösung für dieses Problem haben Guo und seine Kollegen nun einen neuartigen Katalysator entwickelt, der selbst mit Meerwasser effizient arbeiten kann und gleichzeitig für Korrosion und Ablagerungen schützt. Der Katalysator besteht aus dünnen Kohlenstofffäden mit einer Umhüllung aus Kobaltoxid (CoOx). Dieses Material ist ein guter Katalysator für die Wasserspaltung, verliert aber in Meerwasser schnell seine Funktion.
Um dies verhindern, beschichteten die Wissenschaftler diese Katalysatorfäden zusätzlich mit einer hauchdünnen Schicht Chrom(III)-oxid (Cr2O3). „Diese Verbindung ist im gesamten Arbeitsbereich der Meerwasser-Elektrolyse elektrochemisch stabil“, erklären Guo und sein Team. Noch wichtiger jedoch: Das Chrom(III)-oxid ist eine starke Lewissäure – es kann Elektronen und negativ geladene Ionen binden und diese so von den Elektroden fernhalten.
Genauso leistungsfähig wie ein Reinwasser-Elektrolyseur
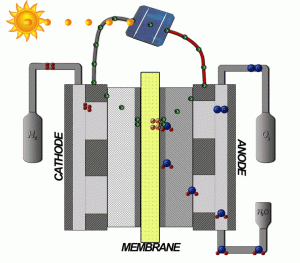
In ersten Praxistests verglichen die Forschenden die Leistungsfähigkeit und Haltbarkeit ihres Elektrolysesystems mit einer gängigen Reinwasser-Anlage, die Platin und Rutheniumdioxid als Katalysator nutzte. Für die Meerwasserspaltung konstruierten sie einen Durchfluss-Elektrolyseur, bei dem ein Titannetz als Elektroden, Cr2O3– CoOx als Katalysator und eine semipermeable Nafion-Membran als Trenner diente. Im Test wurden beide Elektrolyseure von 60 Milliliter Wasser pro Minute durchflossen – in einem Fall von Meerwasser, im anderen von destilliertem Wasser.
Das Ergebnis: Der Meerwasser-Elektrolyseur arbeitete ähnlich effizient und stabil wie das gängige Reinwasser-System. Er erreichte für Wasserstoff und Sauerstoff eine Faraday-Effizienz von 93 und 92 Prozent. „Das deutet darauf hin, dass fast keine Chlorid- und Hydroxid-Beiprodukte gebildet wurden“, berichten Guo und seine Kollegen. Unter anderem deshalb arbeitete das System auch nach mehr als 100 Stunden bei 500 Milliampere pro Zentimeter noch stabil und ohne signifikanten Leistungsverlust.
Zukunftsträchtiger Ansatz
„Damit haben wir normales Meerwasser mit fast 100-prozentiger Effizienz in Sauerstoff und Wasserstoff gespalten – ohne dass eine Vorbehandlung des Meerwassers nötig war“, sagt Koautor Shizhang Qiao von der University of Adelaide. Der Elektrolyseur erreichte mit dem unbehandelten Meerwasser bei 1,87 Volt und 60 Grad eine Leistungsdichte von einem Ampere pro Quadratzentimeter – dies entspreche industriellen Standards, so die Forscher. Zudem bestehe der Katalysator nicht aus teuren Platinmetallen, sondern aus einem nichtedlen, vergleichsweise günstigen Material.
Nach Ansicht der Wissenschaftler eröffnet diese Technologie damit neue Möglichkeiten, Wasserstoff direkt und vergleichsweise günstig aus Meerwasser zu erzeugen – beispielsweise auf Offshore-Anlagen. Guo und seine Kollegen sind bereits dabei, ihr System in größerem Maßstab zu konstruieren, damit es in kommerzielle Anwendungen integriert werden kann. (Nature Energy, 2023; doi: 10.1038/s41560-023-01195-x)
Quelle: University of Adelaide













