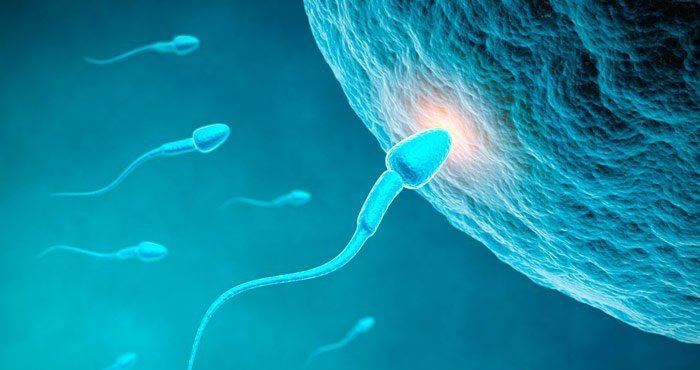
Sie werden in großen Mengen auch im Fortpflanzungstrakt produziert und spielen dort eine Rolle für die Entwicklung der Spermien. „Extrazelluläre Vesikel sind eine einzigartige Form der interzellulären Kommunikation und übertragen Signale, die für Zellprozesse und -funktionen von Bedeutung sind – einschließlich der normalen Heranreifung von Keimzellen“, erklären die Forscher.
Stress verändert interzelluläre Botschafter
Um herauszufinden, ob ihre Theorie stimmt, behandelten Chan und ihr Team männliche Mäuse wiederholt mit dem Stresshormon Corticosteron. Würde sich dies auf die extrazellulären Vesikel der Nager auswirken? Tatsächlich offenbarte sich: Nach der Stressbehandlung veränderten sich die Membranpartikel deutlich. Demnach schrumpften sie nicht nur, auch ihr Inhalt war verändert.
Dies zeigte sich an den in ihnen enthaltenen Proteinen und microRNAs besonders deutlich – diese RNA-Moleküle sind kurze Kopien des Erbguts, die in den Zellen vor allem regulierende Aufgaben übernehmen. „Wir stellten nach der Corticosteron-Behandlung signifikante Veränderungen bei den Expressionsmustern der microRNA fest“, berichten die Wissenschaftler.
Nachhaltiger Effekt
Das Frappierende: Diese Veränderungen blieben selbst dann bestehen, als die Tiere schon lange nicht mehr gestresst waren und sich mehrere Wochen hatten erholen können. „Es handelt sich offenbar um eine nachhaltige programmatische Veränderung in Folge von chronischem Stress“, konstatieren Chan und ihre Kollegen.
Wie aber wirkt sich dies nun auf die Spermien und damit auf den Nachwuchs aus? Das enthüllten weitere Experimente: Kamen die Spermien vor der Befruchtung mit den „gestressten“ extrazellulären Vesikeln in Kontakt, veränderten sie sich – und das beeinflusste die Entwicklung des aus solchen Spermien gezeugten Mäuse-Embryos messbar.
Veränderte Gehirnentwicklung
Konkret stellten die Forscher Veränderungen bei der frühen Gehirnentwicklung fest. Dabei zeigten sich unter anderem signifikante Effekte an Genen, die für synaptische Signalwege und den Transport von Neurotransmittern eine Rolle spielen. „Dies spricht für wichtige Veränderungen der neuronalen Entwicklung, die sich auf die Gehirnfunktion im Erwachsenenalter auswirken könnten“, erklärt das Team.
Außerdem zeichneten sich Veränderungen bei Gengruppen ab, die für Immunprozesse zuständig sind. Zusätzlich identifizierten die Wissenschaftler auch Veränderungen im Plazentagewebe, durch die es vermehrt zu Entzündungs- und Immunreaktionen zu kommen schien.
Folgen für den Nachwuchs unklar
„Unsere Studie zeigt, dass sich das Gehirn des Babys im Mutterleib anders entwickelt, wenn der Vater vor der Empfängnis eine chronische Phase von Stress erlebt hat“, fasst Mitautorin Tracey Bale von der University of Maryland in Baltimore zusammen. „Wir wissen jedoch noch nicht, welche Bedeutung diese Unterschiede haben.“
Erhöht sich dadurch zum Beispiel die Anfälligkeit für mentale Probleme beim Nachwuchs oder verändert sich seine Fähigkeit, mit Stress umzugehen? Zumindest für Letzteres haben die Forscher bereits Indizien entdeckt. So zeigte sich, dass betroffene Mäuse im Erwachsenenalter anders auf psychische Belastungen reagierten als Kontrolltiere.
Stresseffekt auch bei menschlichem Sperma
Während die genauen Effekte der vererbten Stressfolgen noch unklar sind, zeichnet sich aber schon ab: Auch beim Menschen könnten sich chronische psychische Belastungen des Vaters auf den Nachwuchs auswirken. Deutliche Hinweise darauf fanden die Wissenschaftler, als sie Spermienproben von Studierenden analysierten.
Die freiwilligen Probanden gaben über einen Zeitraum von einem halben Jahr monatlich Sperma ab. Außerdem beantworteten sie einen Fragebogen, der ihr Stresserleben im vorangegangenen Monat erfasste. Das Ergebnis: Studierende die im vorherigen Monat stärker gestresst gewesen waren, wiesen Veränderungen in ihrem Sperma auf – vor allem in Bezug auf den microRNA-Gehalt.
Entspannen für die nächste Generation
„Diese Arbeit ist ein weiterer wichtiger Schritt, um grundlegende Mechanismen der Epigenetik zu verstehen“, kommentiert Albert Reece von der University of Maryland. „Es gibt viele Gründe, warum wir versuchen sollten, unsere Stressbelastung zu reduzieren – gerade jetzt, wenn wir gestresster sind als sonst und dies wahrscheinlich auch noch einige Monate lang bleiben werden“, ergänzt Bale mit Blick auf die psychologischen Auswirkungen der Coronavirus-Pandemie.
„Vernünftig mit Stress umzugehen, kann nicht nur unsere mentale Gesundheit verbessern und andere stressbedingte Leiden verringern. Es hilft auch dabei, potenzielle Langzeitfolgen auf das Fortpflanzungssystem zu reduzieren, die künftige Generationen beeinflussen könnten“, so ihr Fazit. (Nature Communications, 2020, doi: 10.1038/s41467-020-15305-w)
Quelle: University of Maryland School of Medicine
1. April 2020
- Daniela Albat