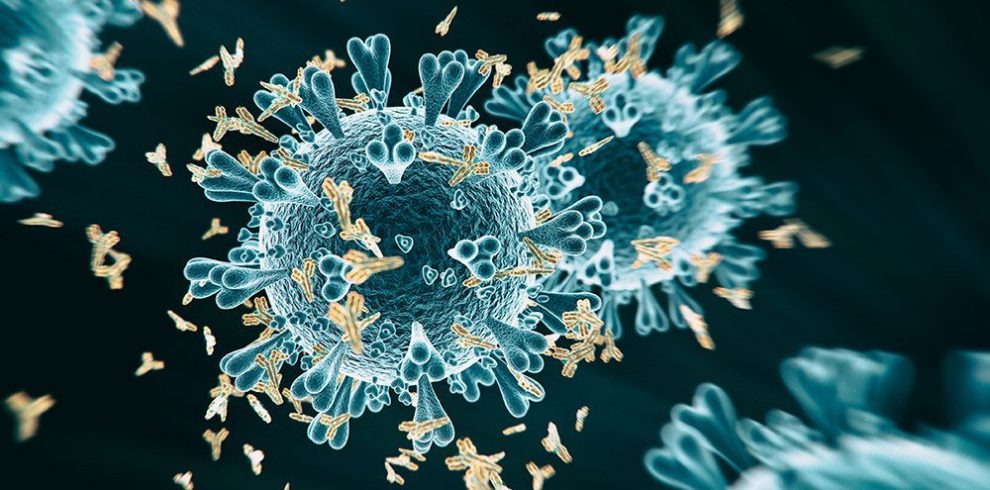
Voraussetzung dafür ist allerdings, dass diese Antikörper an verschiedenen Stellen des Virus ansetzen, ohne sich gegenseitig zu behindern – und dass jeder dieser Immunglobuline auch für sich allein genommen die Virenvermehrung stoppen kann.
Sieben Antikörper-Paare gegen SARS-CoV-2
Ob es solche Antikörper-Paare gibt und wie gut sie auch bei Mutationen von SARS-CoV-2 wirken, haben Johanna Hansen von der US-Firma Regeneron Pharmaceuticals und ihre Kollegen untersucht. Dafür prüften sie zunächst mehr als tausend aus dem Blutplasma von Covid-19-Patienten isolierte Antikörper auf ihre Wirksamkeit gegen SARS-CoV-2. Etwa 40 Kandidaten zeigten in Neutralisationstests eine ausreichend hohe Blockadewirkung.
Bei diesen Antikörpern analysierten die Forscher dann, an welcher Struktur des viralen Spike-Proteins sie sich anlagerten. Bei den potentesten Vertretern waren dies Teile der viralen Rezeptorbindestelle – dem Teil des Proteins, mit dem das Coronavirus an den ACE2-Rezeptor auf der Zelloberfläche andockt. Für einen kombinierten Einsatz kommen jedoch nur Immunglobuline in Frage, die zu zweit ans Virus binden können, ohne dass es zu gegenseitigen Behinderungen kommt.
Tatsächlich wurden Hansen und ihr Team fündig: Sie identifizierten sieben Paare von Antikörpern, die sich keine gegenseitige Konkurrenz bei der Anlagerung ans Virus machten und gleichzeitig eine hohe Neutralisationspotenz besaßen.
Gezielter Test mit „Flucht-Mutanten“
An diesem Punkt setzt die zweite Studie an. Hansens Kollegin Alina Baum und ihr Team haben darin vier dieser Antikörper noch genauer getestet. Dafür prüften sie zunächst, wie gut diese Immunglobuline gegen verschiedene Stämme von SARS-CoV-2 wirken. Das Ergebnis: „Unsere Top-Kandidaten behielten ihre potente Neutralisationswirkung gegen alle getesteten Virenvarianten“, so die Forscher.
Nun folgte der Härtetest: Die Wissenschaftler versetzten Virenkulturen mit geringen, nicht tödlichen Dosen der einzelnen Antikörper. Dies führte schnell dazu, dass die Mutanten am besten gediehen, auf deren Struktur die Antikörper nicht mehr passten. „Einige dieser Mutanten etablierten sich schon in der zweiten Generation der Virenkultur und repräsentierten dann 100 Prozent der Gensequenzen“, berichten Baum und ihre Kollegen. Als Folge konnten die Antikörper nicht mehr an diese Varianten von SARS-CoV-2 binden.
Antikörper im Zweierpack bleiben wirksam
Anders war dies jedoch, als die Forscher ihre Viruskulturen mit Antikörper-Paaren zur Mutation provozierten. „Der Versuch, SARS-CoV-2 in Gegenwart dieses Antikörper-Cocktails zu vermehren, führte nicht zur Dominanz von Flucht-Mutanten“, berichten Baum und ihr Team. Dies galt aber nur für Paare, die keine oder kaum Überlappungen ihrer Bindestellen besaßen. Die Forscher erklären dies damit, dass das Coronavirus in diesen Fällen Mutationen an gleich zwei Stellen entwickeln müsste – und ein solches Zusammentreffen günstiger Mutationen ist sehr unwahrscheinlich.
Nach Ansicht beider Teams demonstrieren ihre Ergebnisse, dass der Einsatz gezielt ausgewählter Antikörper-Paare das Problem der Flucht-Mutationen am besten umgehen kann. „Die Integration solcher Antikörper in einen Antikörper-Cocktail könnte eine optimale antivirale Wirksamkeit bieten, während sie das Risiko einer viralen Mutation minimiert“, konstatieren Hansen und ihre Kollegen.
Allerdings gilt für diese wie für alle anderen zurzeit erforschten Antikörper-Kandidaten: Weitere Tests und Tierversuche müssen nun klären, ob diese Antikörper-Paare auch in vivo wirken. Zudem muss das sogenannte Antibody-Dependent Enhancement ausgeschlossen werden, eine durch nicht gut genug passende Antikörper verursachte Verschlimmerung der Infektion. (Science, 2020; doi: 10.1126/science.abd0827; doi: 10.1126/science.abd0831)
Quelle: American Association for the Advancement of Science
16. Juni 2020
- Nadja Podbregar