Erneuerungstalent: Der Knorpel in unseren Gelenken hat womöglich ein größeres Regenerationspotenzial als gedacht. Denn wie Untersuchungen menschlichen Knorpelgewebes nahelegen, können in den Gelenken doch neue Knorpelproteine gebildet werden – insbesondere im Fußgelenk. Bestätigt sich diese Salamander-ähnliche Fähigkeit zur Regeneration, könnten sich daraus neue Ansätze zur Therapie von Erkrankungen wie Arthrose ergeben.
Verlorenes Gewebe einfach nachwachsen lassen: Während dem menschlichen Körper dies nur bedingt gelingt – zum Beispiel bei Haut und Leber – sind andere Wesen des Tierreichs wahre Regenerationskünstler. So kann die mit Quallen verwandte Hydra jedes verlorene Körperteil binnen kürzester Zeit nachbilden, mancher Meereswurm erneuert bei Bedarf einfach seinen Kopf und für den Axolotl ist selbst durchtrenntes Rückenmark oder verletztes Netzhautgewebe kein Problem.
Doch womöglich besitzen auch wir Menschen mehr solcher „Superkräfte“ als bislang gedacht, wie Ming-Feng Hsueh von der Duke University in Durham und seine Kollegen berichten. Die Forscher haben Hinweise darauf gefunden, dass unser Knorpel über ein unerkanntes Regenerationspotenzial verfügt.
Was weg ist, ist weg?
Gängiger Annahme nach kann der Knorpel in den Gelenken nicht von alleine nachwachsen. Ist dieses Gewebe erst einmal abgenutzt, bleiben oft nur Schmerz und Folgeerkrankungen wie Arthrose. Doch stimmt der Spruch, „was weg ist, ist weg“ in diesem Zusammenhang wirklich? Immerhin haben frühere Studien Stamm- und Vorläuferzellen in Knorpelgewebe gefunden und auch klinische Beobachtungen deuten vereinzelt auf eine Erneuerungsfähigkeit des Knorpels hin.
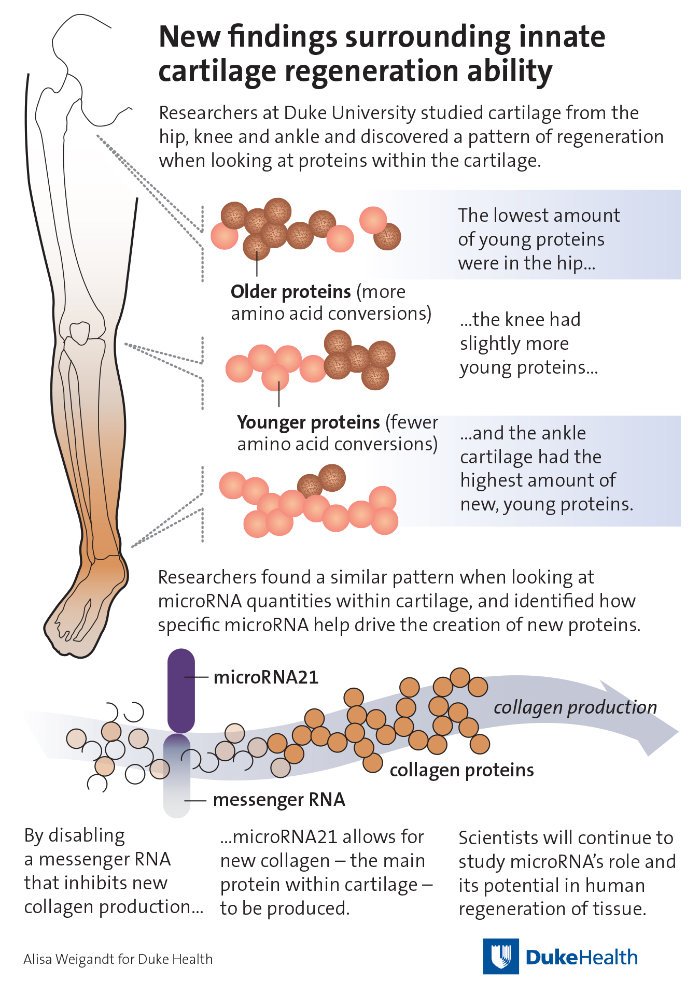
Um mehr darüber herauszufinden, haben Hsueh und sein Team nun menschliche Knorpelproben aus Hüfte, Knie und Fußgelenk unter die Lupe genommen. Die Wissenschaftler konzentrierten sich dabei auf die einzelnen Proteine innerhalb des Gewebes. Sie wollten wissen: Sind diese aus Aminosäuren aufgebauten Makromoleküle alle gleich alt oder lassen sich womöglich Altersunterschiede feststellen, die auf eine Erneuerung des Knorpels hindeuten?
Junge Knorpelproteine im Gelenk
Hsueh und seine Kollegen nutzten dabei die Tatsache aus, dass sich die Bausteine der Proteine im Laufe der Zeit verändern – und zwar mit schöner Regelmäßigkeit. Dank dieser internen „molekularen Uhren“ konnten die Forscher mithilfe der Massenspektrometrie das Alter bestimmter Schlüsselproteine im Knorpel abschätzen.
Tatsächlich stellten sie fest: Es gab sowohl ältere als auch jüngere Proteine. Interessanterweise zeichnete sich dabei ein Zusammenhang zwischen dem Alter des Knorpels und seiner Position im Körper ab. So waren in den Fußgelenken besonders viele junge Proteine enthalten, der Knorpel im Knie war insgesamt eher mittelalt und das Gewebe in der Hüfte bestand aus noch mehr älteren Proteinen.
MicroRNA im Blick
Das Spannende daran: Dieses Muster entspricht dem Regenerationspotenzial unterschiedlicher Körperteile im Tierreich. Denn bei Erneuerungswundern wie Salamander, Zebrafisch und Eidechse wachsen vor allem endständige Körperteile wie die Schwanzspitze oder das Ende der Flossen und Beine leicht nach – also genau jene Stellen, an denen das junge Alter der Proteine auf eine Regenerationsfähigkeit auch beim Menschen hindeutet.
Um dieser auffälligen Übereinstimmung weiter nachzugehen, untersuchten die Wissenschaftler anschließend sogenannte microRNA im Knorpel. Diese für die Genregulation wichtigen Moleküle sind bei Tieren, die für ihr Regenerationstalent bekannt sind, besonders aktiv und scheinen der Schlüssel für nachwachsendes Gewebe zu sein. Auch wir Menschen verfügen über microRNA – doch wie viele dieser Moleküle sind im Knorpel vorhanden?
Schalter für die Kollagenproduktion
Analysen offenbarten, dass auch die Menge aktiver microRNA in Hüfte, Knien und Gelenken unterschiedlich war. Besonders aktiv waren diese Genregulierer dort, wo die Forscher zuvor die jüngsten Proteine entdeckt hatten: in den Gelenken. Außerdem war die Aktivität der microRNA in den oberen Schichten des Knorpels höher als in den tieferliegenden. „Es war spannend festzustellen, dass diese Regler der Gliedmaßen-Regeneration bei Salamander und Co auch beim Menschen die Gewebereparatur zu steuern scheinen“, konstatiert Hsueh.
Tatsächlich konnten er und seine Kollegen schließlich auch einen Mechanismus entschlüsseln, über den microRNA zur Bildung neuen Knorpelgewebes beiträgt. Demnach blockiert die microRNA21 eine Boten-RNA (mRNA), die normalerweise die Produktion neuen Kollagens inhibiert. Als Folge kann nun Kollagen produziert werden – das Strukturprotein ist ein wesentlicher Bestandteil des Knorpels.
Ansatz für Arthrose-Therapie
Die Wissenschaftler glauben, dass ihre Erkenntnisse zum Beispiel erklären könnten, warum die mit fortschreitendem Knorpelabbau verbundene Arthrose in Hüfte und Knien deutlich häufiger vorkommt als in den Fußgelenken. Sie wollen in Zukunft weiter untersuchen, wie bestimmte microRNA-Moleküle die Bildung von Knorpelproteinen im Detail fördern und was dies für die Erneuerungsfähigkeit dieses Gewebes beim Menschen bedeutet.
Bestätigt sich dabei, dass unser Knorpel tatsächlich ein bisher unerkanntes Regenerationspotenzial besitzt, würden sich damit neue Ansätze für die Therapie von Arthrose ergeben. „Wir könnten diese Regulatoren dafür nutzen, um Knorpel in einem betroffenen Gelenk zu regenerieren“, sagt Hsuehs Kollegin Virginia Kraus.
„Innerer Salamander“
Doch die Forscherin geht noch weiter: „Gelingt es uns zu erkennen, was uns im Vergleich zu Salamandern fehlt, könnten wir diese Faktoren in Zukunft hinzufügen und eine Methode entwickeln, Teile verletzter menschlicher Gliedmaßen nachwachsen zu lassen.“ Noch ist die Medizin davon zwar weit entfernt. Immerhin aber deuten die nun veröffentlichten Daten daraufhin, dass unser „innerer Salamander“ größer sein könnte als gedacht. (Science Advances, 2019; doi: 10.1126/sciadv.aax3203)
Quelle: Duke University Medical Center