Umgerüstet für das gezielte Andocken
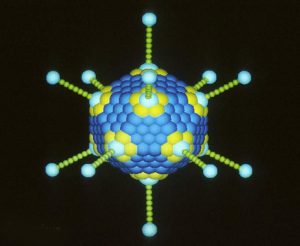
Konkret besteht das SHREAD (SHielded, REtargeted Adenovirus) getaufte Transportvehikel aus dem Adenovirus 5, dem die eigenen viralen Genen entfernt wurden. Stattdessen bekam das Virus in diesem Experiment die Bauanleitung für den gegen Brustkrebs zugelassenen Antikörper Trastuzumab (Herceptin). Damit die Adenoviren gezielt die Krebszellen angreifen, statteten die Forschenden sie mit speziellen Oberflächenmarkern aus, die nur auf die Tumorzellen passen.
Gleichzeitig sorgen weitere Anhängsel dafür, dass die Viren nicht in gesunde Körperzellen und insbesondere das Lebergewebe eindringen können. Das verhindert Nebenwirkungen, wie sie teilweise bei Gentherapie-Versuchen mit Adenoviren beobachtet wurden. Zudem trägt diese Abschirmung dazu bei, dass die viralen Genfähren nicht schon vorzeitig vom Immunsystem abgefangen werden, wie die Wissenschaftler erklären.
Antikörper-Produktion in den Tumorzellen
Im Experiment injizierten das Forscherteam diese SHREAD-Transporter Mäusen, die an Brustkrebs litten. Kontrolltiere erhielten statt der Genfähre das Antikörperpräparat Herceptin in die Blutbahn. Nach einigen Tagen untersuchten Smith und ihr Team, in welchen Zellen und Geweben die viralen Fähren nachweisbar waren. Zudem analysierten sie die Konzentrationen des Herceptin-Antikörpers im Tumor sowie im Blut und anderen Geweben.
Das Ergebnis: Gut 93 Prozent der viralen Fähren hatten wie geplant nur die Tumorzellen befallen und dort ihre Genfracht eingeschleust. 3,7 Prozent waren von Fresszellen verschlungen worden, andere Zelltypen waren dagegen kaum betroffen, wie die Forschenden berichten. In den Krebszellen begann nach wenigen Tagen die Produktion der Antikörper – mit der Folge, dass die Tumore schrumpften, wenn auch noch etwas weniger als bei der normalen Heceptinbehandlung.
Das Positive jedoch: Bei der SHREAD-Therapie produzierten nur die Krebszellen den Antikörper und erzeugten so im Tumor deutlich höhere Konzentrationen als bei einer systemischen Antikörpertherapie. „Wir erzielen eine 21-fach höhere Antikörperkonzentration im Tumor, gleichzeitig 89-fach niedrigere Werte im Blutplasma und eine 2,2-fach niedrigere in der Leber“, berichten Smith und ihr Team.
Einsetzbar auch für andere Krebsmittel
Nach Ansicht des Forschungsteam demonstriert dies, dass diese Vor-Ort-Produktion den Wirkstoff effektiver und gezielter dorthin bringt, wo er wirken soll – direkt in den Tumorzellen. Wie sie erklären, lässt sich das virale SHREAD-Vehikel auch für das Einschleusen anderer Bauanleitungen und Wirkstoffe gegen Krebs einsetzen, darunter auch Medikamente, die für gesunde Körperzellen zu toxisch wären. Weil sie primär in den angegriffenen Krebszellen selbst produziert werden, kommen normale Zellen kaum mit den Mitteln in Kontakt.
„Diese Strategie könnte daher besonders wichtig sein, um adäquate Verabreichungsmethoden für solche Therapeutika zu etablieren, die andernfalls in der Krebstherapie nicht eingesetzt werden könnten“, erklären Smith und ihre Kollegen. Dazu gehören unter anderem bestimmte Proteine, die zurzeit als Biologika gegen Krebs in der Entwicklung sind.
Als Inhalationsmittel gegen Covid-19?
Aber nicht nur gegen Krebs könnten die SHREAD-Viren nützlich sein – im Zuge der Corona-Pandemie wäre sie sogar gegen Covid-19 einsetzbar: „Indem die SHREAD-Behandlung den Patienten über ein inhalatives Aerosol verabreicht wird, könnte unser Ansatz eine gezielte Produktion von Covid-Antikörpern in Lungenzellen zulassen – dort, wo sie am dringendsten gebraucht werden“, erläutert Smith.
„Damit ließen sich Kosten senken, die Zugänglichkeit von Covid-Therapien erhöhen und mit dem Inhalations-Ansatz auch die Verabreichung von Impfstoffen verbessern.“ (Proceedings oft he National Academy of Sciences, 2021; doi: 10.1073/pnas.2017925118)
Quelle: Universität Zürich
19. Mai 2021
- Nadja Podbregar