Genetischer Gegenspieler: Neurowissenschaftler haben eine Genvariante entdeckt, die Risikopatienten vor Alzheimer schützen könnte. Sie senkt die Wahrscheinlichkeit, an Alzheimer zu erkranken, um bis zu 70 Prozent. Träger dieser Genvariante könnten weitgehend vor der Demenz bewahrt bleiben, weil ihre Blut-Hirn-Schranke durchlässiger ist. Dadurch werden schädliche Proteinverklumpungen aus dem Gehirn abtransportiert, bevor sie neurologische Schäden anrichten. Die Erkenntnis könnte auch zu neuen Therapien bei Alzheimer-Demenz verhelfen.
Die genauen Ursachen der Alzheimer-Demenz sind bisher unklar. Möglicherweise spielen je nach Subtyp verschiedene Faktoren eine Rolle. Bekannt ist aber, dass die Erkrankung zum Teil genetisch bedingt ist. Zum Beispiel haben Menschen, die die sogenannte e4-Form des APOE-Gens in ihrem Erbgut tragen, ein deutlich höheres Risiko, an Alzheimer zu erkranken, als Personen ohne dieses Gen. Doch es gibt auch Menschen, die trotz dieses Gens nie Demenzsymptome entwickeln.
Spurensuche bei Risikopatienten
„Anhand dieser resilienten Menschen können wir viel über die Krankheit lernen und darüber, welche genetischen und nicht-genetischen Faktoren vor Alzheimer schützen könnten“, sagt Seniorautor Badri Vardarajan von der Columbia University in New York. „Wir stellten die Hypothese auf, dass diese widerstandsfähigen Menschen genetische Varianten haben könnten, die sie vor APOEe4 schützen.”
Um diese Hypothese zu überprüfen, hat ein Team aus Neurowissenschaftlern um Vardarajan und Erstautor Prabesh Bhattarai das Erbgut von rund 3.500 solcher Risikopatienten genauer untersucht. Die Testpersonen waren über 70 Jahre alt und Träger der APOEe4-Genvariante. Einige waren bereits an Alzheimer erkrankt, andere nicht. Die meisten Teilnehmer lebten in Northern Manhattan in New York und nahmen an einer dort seit über 30 Jahren laufenden Studie zu Alterserkrankungen teil.
Genvariante verändert Blut-Hirn-Schranke
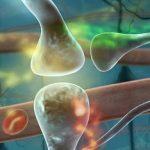
Die Auswertung der DNA-Sequenzen ergab, dass einige Träger der APOEe4-Genvariante ohne Alzheimer-Symptome tatsächlich eine weitere besondere Genvariante tragen. Das bei ihnen veränderte Gen FN1 kodiert für das Protein Fibronektin – eine Komponente der Blut-Hirn-Schranke. Diese reguliert, welche Substanzen aus dem Blut ins Gehirn und umgekehrt gelangen. Bei einigen Alzheimer-Patienten enthält die Blut-Hirn-Schranke allerdings viel größere Mengen Fibronektin als bei gesunden Menschen und ist dadurch undurchlässiger, wie die Neurowissenschaftler erklären.
Nicht so jedoch bei Menschen mit der neu entdeckten Variante des Fibronektin-Gens in ihrem Erbgut: Diese Personen weisen keine erhöhten Fibronektin-Anteile in der Blut-Hirn-Schranke auf. Das scheint sie vor einer Alzheimer-Erkrankung zu schützen, berichten Bhattarai und seine Kollegen.
Abbau schädlicher Proteinklumpen
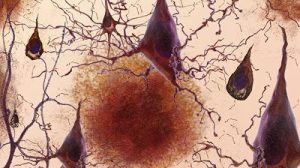
Aber welchen Vorteil hat es, eine durchlässige Blut-Hirn-Schranke mit wenig Fibronektin zu haben? Das Team vermutet, dass dann fehlgefaltete Formen von Amyloid-Proteinen leichter aus dem Gehirn herausgelangen können. Bei Alzheimer-Patienten mit viel Fibronektin in der Blut-Hirn-Schranke sammeln sich diese Amyloid-Proteinen stattdessen im Gehirn an und verklumpen dort, so die Theorie der Forschenden.
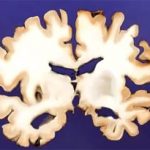
„Überschüssiges Fibronektin könnte die Beseitigung von Amyloid-Ablagerungen aus dem Gehirn verhindern“, sagt Koautor Caghan Kizil von der Columbia University. Mit der Zeit entwickeln sich dadurch Alzheimer-Symptome. „Die Alzheimer-Krankheit kann mit Amyloid-Ablagerungen im Gehirn beginnen, aber die Krankheitssymptome sind das Ergebnis von neurologischen Veränderungen, die nach dem Auftreten der Ablagerungen auftreten“, erklärt er. Bei einem rechtzeitigen Abtransport der Amyloide über die Blut-Hirn-Schranke treten demnach keine Hirnschäden und Symptome auf.
Folgeuntersuchungen an Zebrafischen mit Alzheimer bestätigten diese Hypothese, wie das Team berichtet. Dabei stellten die Neurowissenschaftler außerdem fest, dass die Amyloid-Klumpen im Gehirn der Fische wieder kleiner wurden, wenn der Fibronektin-Anteil in ihrer Blut-Hirn-Schranke reduziert wurde. Die neurologischen Schäden gingen daraufhin ebenfalls zurück. Die Entdeckung untermauert frühere Hinweise, wonach die Blut-Hirns-Schranke und die Blutgefäße des Gehirns bei Alzheimer eine große Rolle spielen.
Um 71 Prozent geringeres Alzheimer-Risiko
Basierend auf den Befunden hat das Forschungsteam die Untersuchungen wiederholt. Daran nahmen über 7.000 weitere Personen über 60 Jahren mit der Risiko-Genvariante APOEe4 teil, überwiegend aus Europa. Auch in dieser Probandengruppe fanden Bhattarai und seine Kollegen Menschen mit schützender Genvariante und ohne Alzheimer-Symptome. „Wir fanden die gleiche Fibronektin-Variante, was unsere Ergebnisse bestätigte“, sagt Vardarajan.
Insgesamt nahmen an den beiden Studien rund 11.000 Testpersonen verschiedener Herkunft mit der APOEe4-Genvariante teil. Menschen, die zusätzlich die Fibronektin-Genvariante trugen, hatten dabei ein um 71 Prozent geringeres Risiko, an Alzheimer zu erkranken, wie die Forschenden berechneten. Bei denjenigen, die dennoch an Alzheimer erkrankten, traten die Symptome immerhin dreieinhalb Jahre später auf als ohne die Fibronektin-Genvariante.
Allerdings ist die vor Alzheimer schützende Genvariante eher selten: Sie kommt nur in etwa ein bis drei Prozent der US-Amerikaner mit dem Risikogen APOEe4 vor. Ob die schützende Fibronektin-Genvariante auch im Erbgut von Menschen ohne Alzheimer-Risikogen APOEe4 auftritt, ist noch nicht bekannt. Insgesamt scheint sie jedoch häufiger vorzukommen als andere, extrem seltene schützende Genvarianten.
Neue Ansatz für Prävention und Therapie
Die neuen Erkenntnisse könnten nun in die Entwicklung von Alzheimer-Therapien eingehen. „Eine Therapie, die auf Fibronektin abzielt und die Wirkung der schützenden Genvariante nachahmt, könnte eine starke Abwehr gegen die Krankheit bieten“, sagt Koautor Richard Mayeux von der Columbia University. So könnte die Krankheit behandelt oder ganz verhindert werden. „Alles, was überschüssiges Fibronektin reduziert, sollte einen gewissen Schutz vor Alzheimer bieten. Ein Medikament, das dies tut, könnte ein bedeutender Schritt vorwärts im Kampf gegen diese Erkrankung sein“, ergänzt Kizil.
Bisherige Behandlungen – über Antikörper-Präparate wie Donanemab oder Lecanemab – zielen darauf ab, die schädlichen Amyloid-Aggregate im Gehirn über das Immunsystem zu attackieren und abzubauen. Das funktioniert zwar sehr gut, bereits bestehende Symptome und Nervenschäden werden dadurch allerdings nicht rückgängig gemacht. Der Therapie-Ansatz in der Blut-Hirn-Schranke könnte jedoch Proteinaggregate verhindern, bevor sie Schaden anrichten. „Möglicherweise müssen wir viel früher mit der Beseitigung von Amyloid beginnen. Wir glauben, dass dies über den Blutkreislauf geschehen kann“, fügt Mayeux hinzu. (Acta Neuropathologica, 2024; doi: 10.1007/s00401-024-02721-1)
Quelle: Columbia University Irving Medical Center