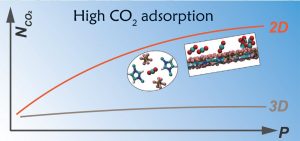
Effektiver Gasfänger: Eine ultradünne Schicht eines flüssigen Salzes könnte das Abscheiden von Kohlendioxid aus der Luft voranbringen, wie eine Studie nahelegt. Demnach kann die 2D-Form solcher ionischen Flüssigkeiten gut zehnmal mehr CO2 binden und ist strukturell robuster als die dreidimensionale Form solcher Salze. Ursache dafür ist eine stabile Schachbrett-Konfiguration, die die Ionen in dieser einschichtigen Verbindung annehmen.
Die CO2-Abscheidung und -Umwandlung (CCU) gilt als wichtige Technologie für den Klimaschutz. Denn das Abtrennen des Kohlendioxids aus Abgasen oder der Umgebungsluft wirkt dem Treibhauseffekt entgegen, vor allem, wenn das CO2 langfristig in Gesteinen oder Baustoffen gebunden wird. Aber auch synthetische Treibstoffe können mittels CO2-Capture und anschließender chemischer Weiterverarbeitung des CO2 erzeugt werden.
Ionische Flüssigkeiten als CO2-Falle?
Doch die Technologien für ein effektives CO2-Capture stehen erst am Anfang. Bisher werden in solchen Anlagen meist flüssige Absorber in Form von Aminen eingesetzt, die aber vergleichsweise viel Energie benötigen, um das gebundene CO2 anschließend wieder freizugeben. Auch metallorganische Gerüstverbindungen oder spezielle Membranen kommen als Absorber in Frage, sind aber erst im Teststadium.
Einen weiteren, vielversprechenden CO2-Absorber stellen nun Yanlei Wang und seine Kollegen von der Chinesischen Akademie der Wissenschaften in Peking vor. Basis ihrer Studie bildet eine ionische Flüssigkeit. Dabei handelt es sich um aus Ionen bestehende Salze, die schon bei Temperaturen von unter 100 Grad schmelzen, aber nur sehr schwer verdampfen. Meist bestehen diese Flüssigkeiten aus organischen, ringförmigen Aminverbindungen wie Imidazolen, die mit einem negativ geladenen, halogenhaltigen Partner kombiniert werden.