„Unmögliches“ Molekül: Chemiker haben erstmals eine aromatische Ringverbindung aus fünf Atomen, aber nur zwei delokalisierten Elektronen erzeugt. Ein so elektronenarmer Aromat galt als nahezu unmöglich und wurde noch nie zuvor erfolgreich nachgewiesen. Das neue Ringmolekül besteht aus Galliumatomen, die über und unter der Ringebene mit zwei Kaliumatomen assoziiert sind. Solche aromatischen Fünfringe könnten die Synthese neuartiger Komplexmoleküle ermöglichen.
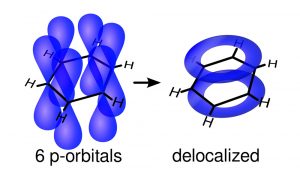
Das Grundprinzip aromatischer Verbindungen entdeckte der Chemiker August Kekulé schon im Jahr 1865 – der Überlieferung nach im Halbschlaf: Er erkannte, dass sich die Kohlenstoffatome im Benzolring einige ihrer Elektronen teilen. Diese sogenannten π-Elektronen sind nicht fest einem Atom zugeordnet, sondern bilden ein über dem gesamten Ring reichendes Orbital – sie sind delokalisiert.
Heute weiß man, dass zwei Drittel aller bekannten chemischen Verbindungen ganz oder teilweise aromatisch sind. Das Gerüst eines solchen Rings kann dabei aus Kohlenstoffatomen bestehen wie beim Benzol, es kann aber auch von anderen Atomen wie Metallen gebildet werden.
Wie groß kann ein Ring mit nur zwei π-Elektronen werden?
Doch wo liegen die Grenzen solcher aromatischen Ringe? Während die Höchstwerte inzwischen Ringe mit 162 π-Elektronen erreicht haben und ein Ende offen scheint, gelten nach unten hin zwei π-Elektronen als absolutes Minimum für einen aromatischer Ring. Bisher wurden solche Minimalringe jedoch nur aus drei oder vier Ringatomen erzeugt, mehr galt als unmöglich. Denn je größer ein Ring wird, desto mehr Atome müssen sich die zwei delokalisierten Elektronen teilen – und desto schwächer wird der stabilisierende Effekt.













