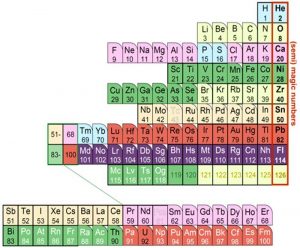
Neue Sortierung: Forscher haben erstmals ein Periodensystem zusammengestellt, in dem die Elemente nach der Füllung ihrer Kernschalen gruppiert werden – und damit nach der Zahl ihrer Protonen. Denn ähnlich wie die Elektronenzahl das chemische Verhalten der Elemente bestimmt, beeinflussen die Kernschalen und ihre „magischen Zahlen“ das Aussehen und Verhalten der Atomkerne – und das macht die neue Anordnung nun sichtbar.
Das Periodensystem der Elemente bildet die Grundlage der Chemie. Denn die Position eines Atoms in dieser Tabelle verrät nicht nur sein Atomgewicht und die Zahl der Protonen im Kern. Sie erlaubt auch Rückschlüsse darüber, wie viele Elektronen es in seiner Hülle trägt und wie es sich daher in Bindungen und chemischen Reaktionen verhält.
Schalen im Atomkern und „magische Zahlen“
Doch die Orbitale der Elektronenhülle sind nicht das einzige Ordnungsprinzip in den Atomen. Forscher vermuten schon länger, dass es auch im Atomkern quantenmechanisch bedingte „Schalen“ gibt, die von den Protonen und Neutronen sukzessive aufgefüllt werden. Analog zu den Elektronenschalen könnten dabei volle Kernschalen energetisch vorteilhaft sein und diesem Atomkern eine größere Stabilität verleihen.
„Wenn diese nuklearen Orbits mit Protonen aufgefüllt sind, bilden sie stabile Kerne – ähnlich wie bei den Elektronenorbitalen die stabilen Edelgase“, erklärt Kouichi Hagino von der Universität Kyoto. Tatsächlich zeigen Beobachtungen, dass Atomkerne mit bestimmten Protonen- oder Neutronenzahlen eine höhere Bindungsenergie besitzen. Bei radioaktiven Isotopen zeigt sich diese „magische Zahl“ in einer längeren Halbwertszeit.