Mit einer speziellen Methode haben Wissenschaftler erstmals die genaue Orientierung der aktiven Zentren eines wichtigen Eiweißkomplexes in der Zelle vermessen. Sie konnten dabei die Struktur des Proteins Ribonukleotid-Reduktase genauer bestimmen, das eine Schlüsselrolle beim Bau der Erbsubstanz DNA spielt.
Die Erkenntnisse der Wissenschaftler ermöglichen neue Einblicke in die Struktur und Funktionsweise dieses lebenswichtigen Proteins. Von einem besseren Verständnis der Arbeitsweise des Eiweißes könnte zukünftig auch die medizinische Forschung profitieren, um Krebsmedikamente weiterzuentwickeln, so die Forscher in der aktuellen Ausgabe der Fachzeitschrift Angewandte Chemie.
Proteinkomplexaus Ribonukleotid-Reduktasen
Als es James Watson und Francis Crick 1953 gelang, die Struktur der Erbsubstanz DNA aufzuklären, war nur wenig darüber bekannt, wie diese in den Zellen zusammengebaut wird. Erst acht Jahre später entdeckten Wissenschaftler mit der Ribonukleotid-Reduktase (RNR) ein erstes Protein, das für den Bau der DNA von entscheidender Bedeutung ist.
Von den Bakterien bis hin zum Menschen übernimmt die RNR den letzten Schritt bei der Bildung der einzelnen DNA-Bausteine. Dabei schließen sich häufig zwei RNR-Proteine zu einem Komplex zusammen. Doch die Funktionsweise dieses Proteinkomplexes ist noch nicht vollständig verstanden – nicht zuletzt deshalb, weil sich die RNR-Proteine nicht ohne weiteres in Aktion beobachten lassen.
Marina Bennati vom Göttinger Max-Planck-Institut für biophysikalische Chemie ist es nun gelungen, den Proteinkomplex direkt in Aktion zu vermessen. Dazu arbeitete die Wissenschaftlerin eng mit Kollegen der Universität Frankfurt und des Max-Planck-Instituts für Bioanorganische Chemie zusammen.
Aktive Proteinkomplexe unter natürlichen Bedingungen untersucht
Erstmalig setzten die Forscher eine neue hochsensitive Methode der Hochfeld-Elektronenspinresonanz-Spektroskopie ein, um die Bewegung und die Struktur der RNR zu untersuchen. „Mit Hilfe dieser neuen Technik können wir aktive Proteinkomplexe unter nahezu natürlichen Bedingungen messen, wie sie auch in der lebenden Zelle vorliegen“, erklärt Bennati.
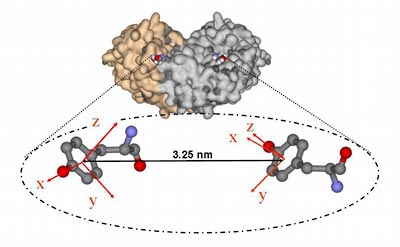
Dabei machen sich die Wissenschaftler zunutze, dass der Proteinkomplex in seinen beiden aktiven Zentren je eine aktivierte Aminosäure enthält. „Mit Hilfe der Elektronenspinresonanz-Spektroskopie messen wir nicht nur den Abstand zwischen den beiden aktivierten Aminosäuren, sondern sehen auch ihre relative Orientierung“, erklärt die Projektleiterin.
Die Methode gibt den Wissenschaftlern dabei nicht nur ein genaueres Bild der Proteinstruktur, sondern erlaubt ihnen auch neue Einblicke in die Funktionsweise des Proteinkomplexes. Entwickelt wurde das dazu verwendete Spektrometer in der Arbeitsgruppe von Professor Thomas Prisner an der Universität Frankfurt.
Ergebnisse wichtig für Entwicklung von Krebsmedikamenten
Proteine in aktivem Zustand in hoher räumlicher und zeitlicher Präzision zu studieren, ist nach Angaben der Wissenschaftler nicht nur für die Grundlagenforschung von Bedeutung. Auch für die medizinische und pharmazeutische Forschung liefert die Beobachtung wichtige Erkenntnisse bei der Entwicklung neuer Medikamente. Da die RNR immer dann gebraucht wird, wenn die Zelle sich teilt oder wenn DNA-Schäden repariert werden müssen, ist das Protein Gegenstand zahlreicher Untersuchungen für die Entwicklung von Medikamenten gegen Krebs.
Von einem verbesserten Verständnis der Funktionsweise und Struktur des Proteins könnte zukünftig auch die medizinische und pharmazeutische Forschung bei der Weiterentwicklung dieser Krebsmedikamente profitieren, so die Chemiker in Angewandte Chemie.
(idw – Max-Planck-Institut für biophysikalische Chemie, 22.02.2008 – DLO)