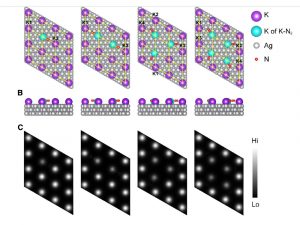
Chemiker haben erstmals einen entscheidenden Schritt der Ammoniaksynthese im Haber-Bosch-Verfahren direkt sichtbar gemacht – die Bindung des Stickstoffmoleküls (N2) an den Katalysator. Im Rastertunnelmikroskop beobachteten sie, wie sich die Moleküle anlagerten und wie dies ihre Ausrichtung und Bindung veränderte. Dieser Schritt ist die Voraussetzung für das Aufbrechen der starken Dreifachbindung im Stickstoffmolekül und damit auch für den restlichen Verlauf der Ammoniaksynthese.
Die vor rund 100 Jahren von deutschen Chemikern entwickelte Ammoniaksynthese mit dem Haber-Bosch-Verfahren ist bis heute die Verfahrensgrundlage bei der Produktion eines Großteils der weltweit eingesetzten Düngemittel, aber auch anderer Chemieprodukte. Durch Druck, Hitze und Katalysatoren wird dabei zunächst die stabile Dreifachbindung des Stickstoffmoleküls geknackt, damit der Stickstoff dann mit Wasserstoff zu Ammoniak (NH3) reagieren kann.
Der Energieaufwand für diese mehrschrittige Synthese ist beträchtlich: Das Haber-Bosch-Verfahren ist für rund ein Prozent des weltweiten Energieverbrauchs und 1,4 Prozent der CO2-Emissionen verantwortlich. Entsprechend groß ist das Interesse an Optimierungen oder Alternativen für diesen Prozess.
Katalysator-Stickstoff-Interaktion unterm Mikroskop
Einen direkten Einblick in einen der entscheidenden Schritte des Haber-Bosch-Verfahrens haben nun Chao Zhang von der University of Pittsburgh und seine Kollegen gewonnen. Sie haben erstmals direkt beobachtet, was bei der Anlagerung des Stickstoffmoleküls an einen der Co-Katalysatoren der Reaktion geschieht. „Bei der Ammoniaksynthese erleichtern Promoter in Form von Alkali-Atomen die Stickstoff-Dissoziation“, erklären sie. „Diese gilt als der limitierende Schritt der Prozesskette.“