Dresdner Forscher haben zahlreiche neue Gene entdeckt, die lenken, wann embryonale Stammzellen pluripotent bleiben – und damit jeden Zelltyp ausbilden können – oder ausdifferenzieren. Die Forscher berichten über die Ergebnisse ihrer neuen Studie in der Fachzeitschrift „Cell Stem Cell.
{1r}
Embryonale Stammzellen sind unsterbliche Multitalente – sie vermehren sich unbegrenzt und sie besitzen das Potenzial, jeden Zelltyp des erwachsenen Organismus auszubilden. Diese Pluripotenz macht sie für die Medizin interessant: Sie könnten als Ausgangsmaterial für hochspezialisierte Zellen – wie zum Beispiel Nervenzellen – genutzt und gezüchtet werden, und nach einer Transplantation kranke und kaputte Zellen oder gar ganze Gewebe und Organe ersetzen.
Für viele Krankheiten ist dieser Therapieansatz jedoch noch Zukunftsvision. Vor allem aber überwiegt das ethische Problem ihrer Gewinnung: Sie werden aus der Blastozyste, dem vier bis sieben Tage altem Embryo, entnommen – und dieser Embryo wird dabei zerstört.
iPS-Zellen als Alleskönner
Bei induzierten pluripotenten Stammzellen (iPS-Zellen) ist das anders. Auch sie sind Alleskönner – pluripotente Zellen. Doch sie haben einen großen Vorteil: Sie werden aus bereits ausdifferenzierten Zellen, zum Beispiel Hautzellen, gewonnen, die Forscher genetisch so verändern können, dass das embryonale Programm wieder eingeschaltet wird. Dies umgeht den ethischen Konflikt, der bei der Gewinnung von embryonalen Stammzellen besteht: Für iPS-Zellen muss kein Embryo zerstört werden.
Erstaunlicherweise braucht man für die Umprogrammierung einer somatischen in eine iPS-Zelle nur wenige Faktoren, manchmal sogar nur einen. Der wichtigste Faktor hierbei wird von dem Gen Oct4 kodiert. So verwandeln sich neuronale Stammzellen zurück zu iPS-Zellen, wenn man artifiziell Oct4 in ihnen exprimiert.
Genomweiter Screen in Säugetierstammzellen
Ein genomweiter Screen in Säugetierstammzellen, den ein Team um Frank Buchholz vom Max-Planck-Institut für Molekulare Zellbiologie und Genetik in Dresden durchgeführt hat, offenbarte nun 296 Gene, die beeinflussen, wie konzentriert das Gen Oct4 in einer Zelle auftritt, ob die Zelle also pluripotent bleibt oder eine Ausreifung zu einer bestimmten Zellart einleitet. Da mithilfe von Oct4 iPS-Zellen herstellt werden können, liefern die Dresdner Forscher damit wichtige Anhaltspunkte, wie der Umprogrammierungsprozess in Zukunft perfektioniert werden kann.
„Genau wegen ihres hohen medizinischen Potenzials wollen wir Stammzellen und iPS-Zellen noch besser verstehen: Welche Faktoren lassen in ihnen das embryonale Programm ablaufen und steuern ihre Pluripotenz?“, sagt Buchholz.
„Nur wenn wir die Balance aus Selbsterneuerung und Ausreifung von Stamm- und iPS-Zellen detailliert und systematisch verstanden haben, können wir für die Zukunft auch wirklich sichere Zellersatz-Therapien ohne Tumor-Risiko entwickeln“, so Buchholz.
Proteinkomplex näher untersucht
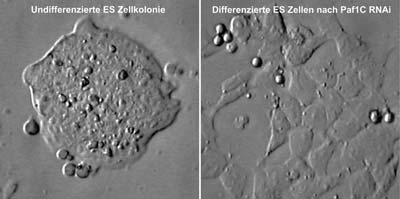
Darüber hinaus haben sich die Forscher einen Proteinkomplex besonders genau angeschaut: Paf1C. „Wir fanden heraus, dass dieser Komplex das Verhalten einer Stammzelle reguliert: Er bindet an viele Promotoren, also die Startbereiche von bestimmten Pluripotenz-Schlüsselgenen, wie zum Beispiel dem Oct4-Gen. Wird Paf1C ausgeschaltet, produziert die Zelle weniger von den Pluripotenz-Schlüsselgenen – die Stammzelle differenziert. Ist Paf1C aber in erhöhten Mengen in der Stammzelle vorhanden, wird eine Ausreifung der Zelle blockiert – die Zelle bleibt embryonal, also pluripotent“, erklärt Buchholz.
(idw – MPG, 06.04.2009 – DLO)