Blick in die Ursuppe: Forschende haben im Röntgenlaser erstmals eine chemische Umwandlung beobachtet, die in der irdischen „Ursuppe“ abgelaufen sein könnte – als erster Schritt zum Leben. Dabei werden Harnstoffmoleküle unter Einfluss energiereicher Strahlung zu hochreaktiven Radikalen. Dies setzt eine Reaktionskette in Gang, durch die einst die Grundbausteine der DNA entstanden. Die Messungen bestätigen zudem, dass diese Harnstoffumwandlung schnell genug abläuft, um sich in Ursuppe durchsetzen zu können, wie das Team in „Nature“ berichtet.
Wie und wo begann das Leben auf der Erde? Bisher ist diese Frage nicht geklärt, aber es gibt zumindest Hinweise darauf, welche Moleküle die Vorstufen zu den ersten Lebensbausteinen bildeten. So bewies schon das berühmte Miller-Urey-Experiment in den 1950er Jahren, dass unter den Bedingungen der Urerde und durch energiereiche Blitze erste Biomoleküle wie Aminosäuren und DNA-Vorstufen entstehen können. Ebenfalls präsent war Harnstoff (CH4N2O), ein einfaches Molekül, das mit Stickstoff und Kohlenstoff die essenziellen Bausteine für DNA-Basen und Aminosäuren liefert.
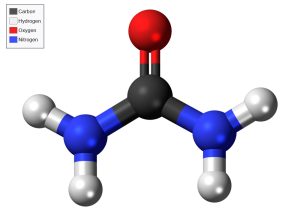
„Harnstoff und seine photoinduzierten Reaktionen sind eine wichtige Säule für die aktuellen Theorien zur Entstehung des Lebens“, erklären Zhong Yin von der ETH Zürich und seine Kollegen. „Wenn Harnstoff ionisierender Strahlung ausgesetzt wird, bildet er Malonsäure, die dann mit weiterem Harnstoff zu verschiedenen DNA-Basen reagieren kann.“ Voraussetzung dafür ist jedoch, dass der Harnstoff zunächst durch energiereiche Strahlung in eine reaktive Form umgewandelt wird.
Zwei Laserpulse und eine Harnstofflösung
Diesen wichtigen ersten Schritt in der photoinduzierten Harnstoff-Reaktionskette haben Yin und seine Kollegen nun erstmals direkt beobachtet. Dafür bestrahlten sie einen mikrometerdünnen Strahl hochkonzentrierter Harnstofflösung mit ultrakurzen Pulsen eines Röntgenlasers. Dabei lieferte ein erster, intensiverer Puls die Energie, um die Reaktion zu starten: Er schlug Elektronen aus einigen Harnstoffmolekülen heraus und ionisierte sie dadurch.