Die dreidimensionale Faltung von Proteinen gibt Forschern nach wie vor Rätsel auf. Die Untersuchung relativ kleiner Proteine könnte sie jedoch einer Lösung dieser Rätsel näher bringen. Deutsche und amerikanische Wissenschaftler haben jetzt einen „Trick“ ersonnen, um einen Einblick auch in bisher verborgene Übergangsstrukturen zu erhalten.
Viele kleine Proteine überqueren bei ihrer Faltung in die dreidimensionale Struktur nur eine einzige Barriere. Diese besteht aus einem Ensemble extrem kurzlebiger Übergangsstrukturen, die nicht direkt beobachtet werden können. Mutationen, die die Faltungsbarriere geringfügig verschieben, ermöglichen jedoch einen indirekten Einblick in die Übergangsvorgänge. Forscher vom Max-Planck-Institut für Kolloid- und Grenzflächenforschung und der Universität von Kalifornien in San Francisco, USA, haben jetzt eine neue Methode entwickelt, mit der die Übergangsstrukturen aus Mutationsdaten rekonstruiert werden können.
Proteine sind Kettenmoleküle, die aus einzelnen Aminosäuren aufgebaut sind. Die genaue Sequenz der 20 verschiedenartigen Aminosäuren innerhalb der Proteinkette bestimmt dabei, in welche spezielle Struktur sich ein Protein faltet. Die dreidimensionale Struktur bestimmt wiederum die Funktion der Proteine, die vom Sauerstofftransport in unserem Blut über die Energieübertragung in unseren Muskeln bis hin zur Stärkung unseres Haares reicht. Während der Evolution wurden die Proteinsequenzen, die in unserer DNA verschlüsselt sind, auf diese Funktionen hin optimiert. Doch nur korrekt gefaltet kann ein Protein seine Funktion erfüllen. Fehler bei der Faltung können zu Proteinzuständen führen, die schwere Krankheiten wie Alzheimer, Parkinson oder das Creutzfeldt-Jakob-Syndrom hervorrufen.
Instabile und kurzlebige Übergangsstrukturen
Während große Proteine ihren endgültigen Faltungszustand über Zwischenzustände erreichen, wurde vor etwa einem Jahrzehnt entdeckt, dass einige kleine Proteine einen erstaunlich direkten Übergang vom ungefalteten in den gefalteten Zustand durchmachen, die so genannte „Zwei-Zustandsfaltung“. Entscheidend bei einer „Zwei-Zustandsfaltung“ ist die Überquerung der Barriere zwischen dem ungefalteten und dem gefalteten Zustand.
Diese Faltungsbarriere besteht aus einer großen Anzahl von extrem kurzlebigen Übergangsstrukturen. Jede dieser Strukturen ist teilweise gefaltet und wird mit gleicher Wahrscheinlichkeit entweder den Faltungsprozess vervollständigen oder sich wieder entfalten. In dieser Hinsicht verhalten sich die Übergangsstrukturen ähnlich einer Kugel auf einem Sattelpunkt. Die Wahrscheinlichkeit, dass die Kugel auf die eine oder die andere Seite des Sattels rollt, liegt hier jeweils bei 50 Prozent.
Da die Übergangsstrukturen sehr instabil sind, lassen sie sich nicht direkt beobachten. Um die Zwei-Zustandsfaltung dennoch erforschen zu können, erzeugt man Mutanten eines Proteins. Diese Mutanten unterscheiden sich vom ursprünglichen Protein, dem „Wildtyp“, in einer einzelnen Aminosäure. Die überwiegende Mehrzahl dieser Mutanten falten zwar in dieselbe dreidimensionale Struktur wie der Wildtyp. Doch die Mutationen verändern geringfügig die Faltungsbarriere und damit auch die Faltungszeit, das heißt die Zeit, die ein ungefaltetes Protein zur Überquerung der Barriere benötigt.
Faltungszeit als Indiz
Üblicherweise werden bei der Rekonstruktion des Faltungsprozesses die Mutationen einzeln betrachtet – eine große Anazhl von Mutanten ist dazu notwendig. Ändert eine Mutation die Faltungszeit nicht, so geht man davon aus, dass die mutierte Aminosäure im Übergangszustand noch unstrukturiert ist. Verändert hingegen eine Mutation die Faltungszeit, so spricht man davon, dass die mutierte Aminosäure im Übergangszustand bereits teilweise oder vollständig strukturiert sei.
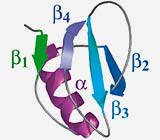
Diese herkömmliche Rekonstruktionsmethode führt jedoch häufig zu Widersprüchen. Beispielsweise haben 20 verschiedene Mutationen in der α-Helix des Proteins Chymotrypsin Inhibitor 2 (CI2) ganz verschiedene Auswirkungen auf die Faltungszeit. Naiv betrachtet würde das dann bedeuten, dass einige Aminosäuren der Helix im Übergangszustand strukturiert sind, während benachbarte Aminosäuren noch unstrukturiert sind. Das ist jedoch nicht konsistent, da die Stabilisierung einer Helix kooperativ erfolgt und mehrere Windungen erfordert, in denen die Aminosäuren eine helikale Struktur annehmen.
Alle auf einmal statt einzeln
Eine völlig neue Rekonstruktionsmethode von Übergangszuständen hat nun ein Forscherteam des Max-Planck-Instituts für Kolloid- und Grenzflächenforschung und der Universität von Kalifornien in San Francisco in einem in der Fachzeitschrift PNAS erschienenen Artikel vorgeschlagen. Anstatt die Mutationen einzeln auszuwerten, werden bei dieser Methode sämtliche Mutationen innerhalb einer kooperativen Substruktur, beispielsweise einer Helix, gemeinsam betrachtet. Im Falle der α-Helix des Proteins CI2 führt das zu einem konsistenten strukturellen Bild, in dem die Helix im Übergangszustand vollständig ausgebildet, jedoch noch nicht an das β-Faltblatt angelagert ist.
Die Max-Planck-Wissenschaftler planen nun, komplette Übergangszustände aus Mutationsdaten zu rekonstruieren. Eine wichtige Voraussetzung dafür ist, die kooperativen Untereinheiten eines Proteins in atomistischen Modellen zu identifizieren. Letztlich können uns nur die Übergangszustände verraten, wie kleine Proteine ihren Weg in die dreidimensionale Struktur finden.
(MPG, 13.10.2005 – NPO)