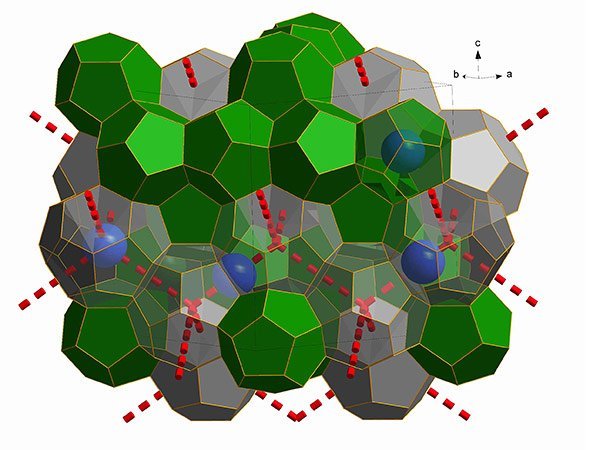
Ein Käfig aus Wasser: Forscher haben eine neue Konfiguration von Wassereis entdeckt. In diesem bilden die Wassermoleküle einen Käfig, in dem andere Moleküle eingeschlossen werden können. Bedeutsam ist diese Entdeckung deshalb, weil diese Eiskäfige auch das Methanhydrat bilden – die Verbindung, in der Millionen Tonnen Methangas im Meeresgrund lagern. Die Kenntnis der Eisstruktur könnte helfen, die Stabilität der Methanhydrate besser zu verstehen, so die Forscher im Fachmagazin „Nature“.
Methanhydrate entstehen nur bei relativ hohem Druck und niedriger Temperatur, wie sie beispielsweise am Meeresgrund der Kontinentalhänge herrschen. Unter diesen Bedingungen werden Methangas-Moleküle in einer Art Käfig aus Wassereis eingeschlossen. Sobald jedoch die Temperaturen steigen, löst sich dieser Käfig auf und das Methangas wird frei – eine Entwicklung, die zurzeit durch den Klimawandel vorangetrieben wird.
Gleichzeitig bildet das Methan in diesen Gashydraten eine potenzielle Energiequelle, denn es ist chemisch nichts anderes als Erdgas. Bisher fehlen aber Ideen dazu, wie sich dieses aus den Hydraten lösen lässt, ohne ganze Meereshänge zu destabilisieren. Ein Grund dafür ist das Eis dieser Hydrate: Zwar war dessen Struktur theoretisch bekannt, es galt aber als unmöglich, die fragilen Eiskäfige ohne Inhalt zu erzeugen oder zu erhalten. Dadurch konnten die Eigenschaften dieser Eisform auch nicht näher erforscht werden.
Leere Käfige im kalten Vakuum
Andrzej Falenty von der Universität Göttingen und seinen Kollegen ist nun erstmals die Synthese dieser Wassereis-Form gelungen – und sie entpuppte sich als völlig neue Eisform. Das von ihnen entdeckte Eis XVI ist die 17. bekannte Struktur des Wassereises. Mit einer Dichte von nur 0,81 Gramm pro Kubikzentimeter ist es zudem diejenige mit der geringsten Dichte. Die Wassermoleküle bilden in dieser Eisform eine hochgradig symmetrische Struktur aus Käfigen, die Fremdmoleküle und Atome einfangen können, um Gashydrate und ähnliche Verbindungen zu bilden.